Авторы: Свительман Мария, глава отдела аналитики, ДМ 365
Гречаниченко Екатерина, Менеджер по медицинским исследованиям, Натива
Стратегический вектор развития индустрии здравоохранения, основанный на этических принципах современного общества, лекарственные средства должны быть не только эффективными и безопасными, но и доступными для потребителей.
Риск-ориентированный подход в клинических исследованиях, отраженный в новой редакции GCP R2 отражает этот тренд как нельзя лучше – меньше ресурсов при сохранении, а зачастую и улучшении качества проведения клинических исследований.
Аббревиатура RBM знакома нам всем. На эту тему в последние десять лет выпущено много статей и материалов, проведены бесчисленные конференции и обсуждения.
Многие знают, немногие делают. Почему? Безусловно, любые перемены - это испытание и труд. В этой статье мы делимся с вами своим опытом внедрения RBM.
Вызовы
При планировании и проведении исследований III фазы мы сталкиваемся с привычными сложностями:
- высокие расходы на мониторинг и операции
- ограниченные ресурсы
Как следствие - увеличивается стоимость лекарственного средства и отодвигается срок его вывода на рынок.
2020 год привнес дополнительный фактор, связанный с пандемией COVID-19, - затруднение или полная невозможность очного мониторирования центров, что еще больше затягивает и удорожает проведение исследований.
Зачем нам это было нужно
Мы столкнулись с теми же трудностями и начали анализировать возможные пути выхода из сложившейся ситуации. Решением было однозначно введение RBM-модели.
Это решение было принято еще до начала пандемии - но пандемия ускорила и расширила способы его реализации.
Как мы принимали решение
Мы преследовали конкретную цель: ускорить и удешевить процесс мониторирования при сохранении или росте качества получаемых данных.
Поэтому основной задачей было изменить процесс, но оставить на прежнем высоком уровне:
- безопасность субъектов исследования,
- целостность и качество собираемых данных,
- качество исследуемого продукта.
Приступив к задаче, мы внимательно изучили:
- российские и международные регуляции (FDA, EMEA),
- опыт других компаний,
- наш предыдущий опыт внедрения и работы с RBM.
Был выработан комбинированный подход:
- внедрение риск-ориентированной методологии
- смещение фокуса мониторирования с очного на удаленное
- центральный мониторинг данных
- разработка дополнительных инструментов аналитической отчетности.
Такой подход требовал согласования внутри совместной команды Натива и Data Management 365, со Спонсором исследования и даже ЛЭКами. Разумеется, это было выполнено до начала внедрения подхода в первом проекте.
Сколько у нас было времени на переключение
Это был, безусловно, один из главных вызовов - на идущем исследовании в возможно кратчайшие сроки внедрить новый подход к мониторированию.
Конечно, нам помогла гибкая платформа MainEDC™, обладающая техническими возможностями внедрения RBM.
Объединенная команда Натива и Data Management 365 выработала план перехода
Мы разбили процесс на этапы:
- идентифицировать, оценить и приоритизировать риски, связанные с переходом на альтернативные принципы мониторирования
- определить методы и процедуры, позволяющие уменьшить вероятность реализации рисков
- определить процедуры, которые должны быть произведены в случае реализации рисков
- определить необходимый и достаточный объем документации
- оценить возможности создания операционно-программного комплекса
- внести необходимые изменения и дополнения в систему
- валидировать решение
- обучить команду проекта
- go live!
Пошаговая инструкция для тех, кто идет за нами
Определение стратегии RBM
Подразумевается, что Мониторы исследования будут проводить удаленную верификацию определенного набора данных для каждого субъекта в каждом центре, при этом объем проверяемых и верифицируемых данных будет зависеть от текущего уровня оценки центра.
По окончании периода запрета на посещение центров также будет проведена он-сайт верификация определенного объема данных, также в зависимости от уровня оценки центра.
Идентификация и оценка рисков
Мы идентифицировали риски, сгруппировав их по типу:
- безопасность субъектов исследования,
- целостность и качество собираемых данных,
- качество исследуемого продукта.
Далее была произведена оценка рисков по следующим параметрам:
- Серьезность риска
- Вероятность реализации риска
- Возможность обнаружения реализовавшегося риска.
В итоге для каждого риска был определен его приоритет.
Далее мы определили процедуры по снижению вероятности реализации каждого риска и устранению последствий.
Реорганизация бизнес-процессов
Для внедрения RBM и удаленного мониторинга, внутренние процессы компании Натива претерпели изменения. Было решено разработать документы, среди которых:
- Подробное описание стратегии RBM, где доступным для сотрудников медицинского отдела языком описывались цели, процедуры, риски удаленного мониторинга, а также общая информация по работе с данными;
- Пошаговая инструкция по работе с центрами, включающая в себя процедуру методики мониторирования центров, все необходимые для работы мониторов планы, схемы и шаблоны;
- Произведено обновление мониторингового плана и внутренних процедур компании.
При создании пакета мы учли, что документация может быть обновлена или переработана при необходимости.
Идентификация критических данных
Важнейшими факторами, влияющими на перечень и приоритет возможных рисков в исследовании, являются:
- данные по безопасности субъектов исследования
- данные для анализа первичных и вторичных точек протокола.
После консультации со статистиками проекта мы определили перечень критических данных нашего исследования, алгоритм и формат их проверки еще в рамках плана валидации данных.
На этом этапе мы дополнительно обозначили события-триггеры, запускающие проверку критических данных.
Процедуры оценки центров (site health assessment)
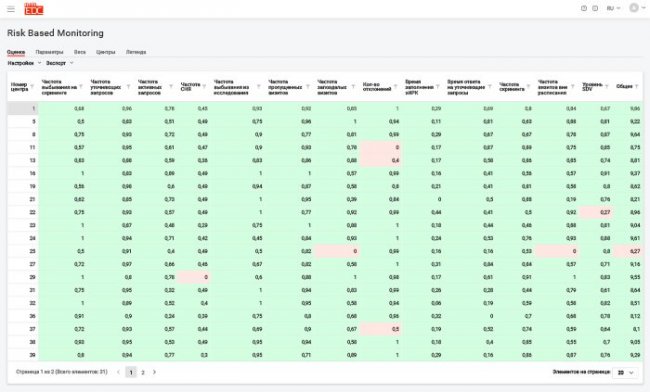
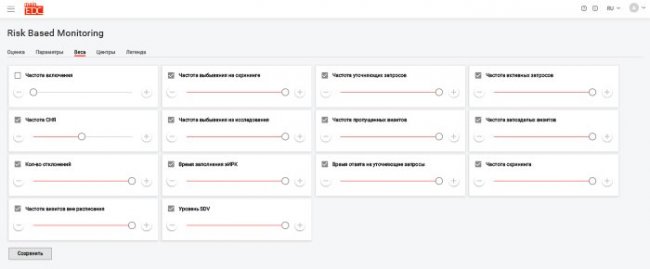
Мы выработали перечень параметров оценки центров на основании данных, внесенных в MainEDC™, и назначили каждому параметру определенный вес.
Далее мы типизировали процедуры оценки:
- первичная
- рутинная (периодическая)
- внеплановая - вызванная определенным событием.
В процессе первичной оценки центра мы устанавливали входные значения по каждому параметру. И при повторной оценке заново их взвешивали, делая вывод о том, как изменяется суммарная оценка центра.
В случае реализации одного или нескольких рисков, определенных ранее, мы проводили внеплановую проверку. Также в этом случае мы увеличивали вес параметра, соответствовавшего реализовавшемуся риску.
В зависимости от результатов проверки, каждому центру присваивался определенный статус. И далее в зависимости от присвоенного статуса и возможности удаленного мониторирования определялся режим работы с центром:
- необходимый масштаб SDV для каждого конкретного центра (в % от общего количества точек данных, вплоть до 100%)
- необходимость очной ре-верификации центра
- глубина Центрального Мониторинга.
Затем мы определяли дату следующей проверки и приоритет очного мониторингового визита.
Внесение необходимых изменений в MainEDC™
Мы проанализировали данные, которые должны помогать в принятии решений при оценке центра:
- состав данных и их представление в системе
- действия, которые могут быть произведены с данными
- разработали статистический базис для проведения оценки центра - линейная нормализация параметров и поиск выбросов
- реализовали и валидировали выбранное решение - от написания требований до приемочного тестирования Натива
- провели тренинги для мониторов Натива
Go live!
После одобрения Натива инструмент RBM был перенесен на рабочую среду системы.
Что у нас получилось
Мы достигли поставленной цели. Срок и стоимость проведения исследования уменьшены, пандемия не привела к остановке процессов в исследовании.
Мы оптимизировали свои бизнес-процессы и обкатали их настолько, чтобы масштабировать новый подход на другие проекты Натива.
Мы получили совершенный гибкий рабочий инструмент, отвечающий нашим ожиданиям и поставленным целям.
Качество получаемых данных не только осталось на заданном уровне, а даже повысилось.
Драматически упала нагрузка на мониторов и врачей. Теперь фокус специалистов направлен туда, где потенциально могут быть проблемы с данными.
Мы видим воодушевление команды мониторов!
Ссылки
Oversight of Clinical Investigations — A Risk-Based Approach to Monitoring (Guidance for Industry AUGUST 2013) https://www.fda.gov/regulatory-information/search-fda-guidance-documents/oversight-clinical-investig...
A Risk-Based Approach to Monitoring of Clinical Investigations Questions and Answers
(Draft Guidance for Industry MARCH 2019) https://www.fda.gov/regulatory-information/search-fda-guidance-documents/risk-based-approach-monitor...
Reflection paper on risk based quality management in clinical trials (18 November 2013 EMA/269011/2013 Compliance and Inspection) https://www.ema.europa.eu/en/documents/scientific-guideline/reflection-paper-risk-based-quality-mana...




 1
1 2
2 3
3 4
4


Комментарии (0)