Журнал "Медицинский совет" №1/2024
DOI: 10.21518/ms2023-470
А.Н.
Завьялова, В.П.
Новикова, М.Н.
Яковлева; Санкт-Петербургский
государственный педиатрический медицинский университет
Первичная саркопения характеризует старческую дряхлость. Вторичная саркопения может встречаться как у взрослых, так и у детей с тяжелой соматической или хирургической патологией. Моделью изучения саркопении у детей могут быть пациенты с детским церебральным параличом с отличным от типично развивающихся детей развитием мышц. В лекции показан механизм развития саркопении, диагностические критерии для взрослых пациентов, представленные в согласительных документах, а также аналоги диагностических шкал, используемых в детской практике. Полностью показаны шкалы сестринской диагностики саркопении у детей «Шалтай-Болтай» и оценки риска падения Морзе. Для максимальной объективизации двигательной активности детей в зависимости от возраста предложены семь вариантов оценки общей моторики, три из которых можно использовать для подросткового и юношеского возраста. Диагностика саркопении у детей перекликается с диагностикой нутритивного статуса у пациента. Объективно саркопению можно диагностировать с использованием двухэнергетической рентгеновской абсорбциометрии, компьютерной или магнитно-резонансной томографии, метода биоимпедансометрии и ультразвукового исследования. Диагностика саркопении у детей методом биоимпедансометрии предложена авторами, получен евразийский патент. На основании объемов жировой и активной клеточной ткани в компонентном составе тела при сочетании доли жировой массы от 40,5% и выше и активной клеточной массы 37% и ниже диагностируют саркопению, а при сочетании доли жировой массы 30,5% и выше и активной клеточной массы от 37 до 43,5% диагностируют пресаркопению. Представлены варианты профилактики саркопении, в том числе запатентованные. Мультидисциплинарный подход к работе с пациентом с саркопенией включает в себя на фоне лечения основного заболевания полноценное питание, восстановление микрофлоры кишечника и двигательной активности пациента.
Для цитирования: Завьялова А.Н., Новикова В.П., Яковлева М.Н. Саркопения у детей: лекция. Медицинский Совет. 2024;(1):245–253. https://doi.org/10.21518/ms2023-470
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Sarcopenia in children: Lecture
Anna N. Zavyalova, Valeriya P. Novikova, Milena N. Yakovleva; St Petersburg State Pediatric Medical University
Primary sarcopenia characterizes frailty of old age. Secondary
sarcopenia can occur in both adults and children with severe somatic or
surgical pathology. A model for studying sarcopenia in children can be patients
with cerebral palsy, whose muscle development differs from typically developing
children. The lecture presents the mechanism of the development of sarcopenia,
diagnostic criteria for adult patients presented in consent documents, as well
as analogues of diagnostic scales used in pediatric practice. The diagnosis of
sarcopenia in children has something in common with the diagnosis of the
patient’s nutritional status. Diagnosis of sarcopenia in children using
bioimpedansometry method was proposed by the authors, and a Eurasian patent was
received. Based on the volumes of adipose and active cellular tissue in the
component composition of the body: with a combination of a percentage of fat
mass of 40.5% and above and a percentage of active cell mass of 37% and below,
sarcopenia is diagnosed, and with a combination of a percentage of fat mass of
30.5% and above and percentage of active cell mass from 37% to 43.5% is
diagnosed as presarcopenia. Options for preventing sarcopenia are presented,
including patented ones. A multidisciplinary approach to working with a patient
with sarcopenia includes, while treating the underlying disease, nutritious
nutrition, restoration of the intestinal microflora and motor activity of the
patient.
For citation: Zavyalova A.N., Novikova V.P., Yakovleva M.N. Sarcopenia in children: Lecture. Meditsinskiy sovet = Medical Council. 2024;(1):245–253. (In Russ.) https://doi.org/10.21518/ms2023-470
Conflict of interest: the authors declare no conflict of interest.
Введение
Саркопения – прогрессирующее
генерализованное заболевание скелетных мышц с ухудшением качества мышечной
архитектуры, снижением функциональной возможности мышц, предсказывающее
неблагоприятный исход [1]. В 1989 г. Розенберг ввел в обиход
этот медицинский термин [2], состоящий из греческих корней
sarco (плоть) и penia (недостаток), как возрастную потерю мышц [1–3]. Суть этого состояния – в
развивающемся клиническом и функциональном состоянии мышц с относительным
увеличением жировой массы по отношению к мышечной (или безжировой) массе [1–4].
Необходимо отметить, что саркопеническое состояние мышц может сопровождаться
как ожирением, так и истощением [5–7]. В любом случае саркопению
необходимо расценивать как недостаточность питания пациента [1, 4].
С
2016 г. саркопения официально признана заболеванием мышц с диагностическим
кодом M62.84 по Международной классификации болезней 10-го пересмотра, который может использоваться для выставления счетов
за лечение. Наиболее
изучено состояние саркопении у взрослых, изданы согласительные документы с
пошаговой диагностикой. Все согласительные документы основываются в целом на
диагностике первичной саркопении [1, 2].
Первичная саркопения
развивается постепенно и исподволь в процессе старения, ее еще называют
дряхлостью. В основе ее лежат старческие изменения организма, связанные со
стоматологическими проблемами пожилых людей, возрастными изменениями
желудочно-кишечного тракта и возрастными изменениями микробиома кишечника,
результатом которых будет функциональная несостоятельность мышц и их низкая работоспособность
[1, 3, 4]. В то же время похожие изменения
происходят в мышцах при тяжелых заболеваниях, сопровождающихся длительным
обездвиженным состоянием. В этом случае развивается вторичная саркопения,
характеризующаяся неблагоприятным исходом как для прогноза заболевания, так и
для жизни [4, 6, 8].
Вторичную саркопению
диагностируют у лиц, проводивших длительное время в невесомости. Вторичная
саркопения развивается вне зависимости от возраста, у молодых людей и также
детей [1, 2, 4].
Модель развития
саркопении
Рисунок 1. Механизм развития саркопении у детей
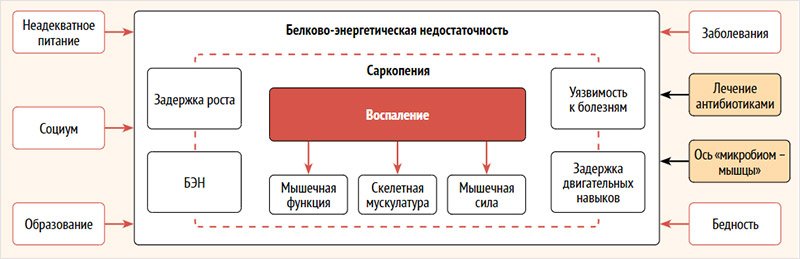
БЭН – Белково-энергетическая недостаточность.
Существует несколько
механизмов развития саркопении и ее прогрессирования (рис. 1). В основе
развития мышц и поддержания их активности лежит синтез белка, протеолиз,
полноценность нервно-мышечной передачи, а также содержание жира и
соединительной ткани в мышцах. Вклад каждого из этих механизмов меняется с
течением времени, возраста пациента и обстоятельств. У лиц пожилого возраста
преобладающие механизмы несколько отличаются от таковых у типично развивающихся
детей. Детский церебральный паралич (ДЦП) изначально оказывает влияние на
развитие мышечной ткани с истощением ее мышечного слоя и увеличением
соединительно-тканных структур относительно здоровых типично развивающихся
сверстников [6]. Само заболевание ДЦП не является
прогрессирующим, однако изменения в мышцах прогрессируют с возрастом и
ухудшением двигательной активности [9–12]. Маломобильные пациенты по мере
взросления реализуют саркопению [6, 12, 13].
Наиболее часто о
саркопении стали вспоминать в контексте перенесенной новой коронавирусной инфекции
[14].
Патофизиология
Взаимодействие
множества факторов и механизмов, включая гормональный фон, регулирующий
анаболические процессы, уровень витаминов и в частности витамина D, физическая активность, диетические
пристрастия и наличие низкоинтенсивного воспаления ведут к развитию саркопении
и влияют на ее тяжесть [15].
На ультраструктурном
уровне скелетные мышцы состоят как из сократительной (актин и миозин), так и из
неконтрактной ткани (в основном коллагена). Сократительные ткани, или мышечные
волокна, отвечают за генерацию моментов, которые приводят к движению суставов и
функциональной деятельности, такой как походка. Сократительная ткань – это
силообразующая ткань, которая вызывает движение. Эти волокна состоят из пучков
миофибрилл – субклеточных органелл длинных, последовательно расположенных
саркомеров, каждый из которых содержит актиновые (тонкие) и миозиновые
(толстые) миофиламенты, которые скользят друг по другу во время сокращения
мышц. В норме сократительные элементы обладают высокой степенью метаболизма и
способствуют метаболическому балансу в организме. Малоподвижность из-за болезни
или образа жизни на фоне неправильных стереотипов питания и минимальных
изменений гормонального фона приведет к патологическим изменениям в
нервно-мышечных соединениях, нарушению капиллярного кровотока, снижению
способности к восстановлению и регенерации из-за уменьшения количества мышечных
клеток-сателлитов, инфильтрации воспалительными клетками и развитию
окислительного стресса. Результатом будет превышение деградации мышечного белка
над его синтезом. Кроме того, окислительный стресс и митохондриальная
дисфункция вызовут метаболические нарушения, такие как резистентность к
инсулину, что приведет к количественным и качественным нарушениям в скелетных
мышцах и развитию саркопении [16, 17]. Уровень цитокинов при развитии
саркопении неоднородно повышается [18]. Таким образом, в результате
воспаления анаболизм мышечных волокон замедляется, а катаболизм усиливается. На
клеточном уровне это проявляется в уменьшении площади поперечного сечения
мышечных волокон, снижении иннервации, изменении пропорции быстрых и медленных
двигательных единиц [19]. Липиды накапливаются в скелетной
мускулатуре, что приводит к митохондриальной дисфункции, повышению продукции
активных форм кислорода, резистентности к инсулину, повышенной секреции
миокинов (миостатина и ирисина), что усугубляет окислительный стресс и
поддерживает воспаление [19, 20]. Выявлено, что уровень миостатина,
подавляющего рост и дифференцировку мышечной ткани, у пациентов с саркопенией
значительно выше, чем у людей, не страдающих данным заболеванием [21, 22], а уровень ирисина снижается [23]. Таким образом, под влиянием этих
миокинов мускулатура утрачивается и заменяется жировыми прослойками.
Порочный круг саркопении представлен
на рис. 2.
Рисунок 2.
Порочный круг саркопении
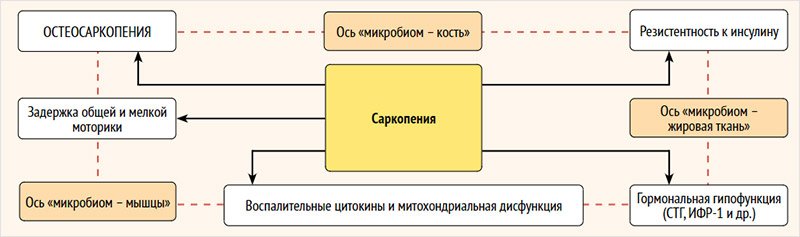
СТГ – соматотропный гормон; ИФР-1 – инсулиноподобный фактор роста 1.
Скрининговая
диагностика саркопении
Критерии диагностики
саркопении у взрослых представлены в первом и втором консенсусе EWGSOP2 (European
Working Group on Sarcopenia in Older People) [1, 3]. Диагноз основывается на сочетании
двух критериев из трех: низкой мышечной массы, низкой мышечной силы и низкой
физической работоспособности [1, 3]. Обосновано это отсутствием
линейной взаимосвязи между мышечной массой и мышечной силой. В втором
консенсусе основную роль в критериях диагностики отвели именно низкой мышечной
силе как основной детерминанте [1]. В то же время малое количество
мышечной массы и худшее качество мышц (мышечную активность) можно измерить. При
этом авторы отмечают, что точно измерить эти показатели затруднительно. Для
определения тяжести саркопении у взрослых предлагают использовать оценку
физической работоспособности [1].
Для определения
физической работоспособности предложены стандартизированные опросники. Рабочая
группа EWGSOP2
предлагает диагностировать саркопению у взрослых с использованием SARC-F (Strength, Assistance with walking, Rising from chair, Climbing stairs and Falls) [1], оценивая чувство слабости,
скорость походки, трудности подъема со стула, а также подъема по лестнице и
опыте падений. Анкета SARC-F высокоспецифична для прогнозирования низкой
мышечной силы, нацелена на выявление тяжелых случаев саркопении. Аналогом
скрининга SARC-F в детской практике может служить
шкала сестринского ухода по оценке риска падения «Хампти-Дампти» (The Humpty Dumpty Scale), или «Шалтай-Болтай» (табл. 1) [24].
Таблица 1.
Шкала сестринской диагностики саркопении у детей «Шалтай-Болтай» [24]
Параметр | Критерии | Баллы |
Возраст | Младше 3 лет | 4 |
От 3 до 7 лет | 3 | |
От 7 до 13 лет | 2 | |
От 13 до 18 лет | 1 | |
Пол | Мужской | 2 |
Женский | 1 | |
Диагноз / отягчающие обстоятельства | Неврологические нарушения | 3 |
Психологические и поведенческие расстройства (гиперактивность, гипервозбудимость и т. д.) | 2 | |
Другое | 1 | |
Когнитивные расстройства | Не осознает своих ограничений | 3 |
Забывает об ограничениях | 2 | |
Ориентируется в собственных способностях | 1 | |
Факторы окружающей среды | В анамнезе случаи падения с детских или взрослых кроватей | 4 |
Пациент использует вспомогательные средства: костыли, ходунки, трость, коляска | 3 | |
Лежачий пациент / на руках (у мамы или другого ухаживающего лица) | 2 | |
Пациент ходит самостоятельно | 1 | |
Состояние после операции/седации/анестезии / инвазивной процедуры | До 24 ч | 3 |
До 48 ч | 2 | |
Более 48 ч / не проводилось | 1 | |
Использование медикаментов | Одновременное применение медикаментов (2 и более): – седативные (за исключением пациентов отделения анестезиологии, реанимации, интенсивной терапии, находящихся в медикаментозной седации и под действием миорелаксантов): диазепам (Реланиум); – снотворные; – противосудорожные препараты: карбамазепин, вальпроевая кислота (Конвулекс, Депакин, Энкорат), ламотриджин (Ламиктал), фенитоин (Дифенин); – барбитураты: фенобарбитал, бензобарбитал; – фенотиазины: хлорпромазин (Аминазин), левомепромазин (Тизерцин); – антидепрессанты; – слабительные/диуретики: лактулоза (Дюфалак), фуросемид (Лазикс), маннитол (Маннит), ацетазоламид (Диакарб); – наркотики: морфин, фентанил, тримеперидин (Промедол) | 3 |
Использование 1 медикамента из вышеперечисленных групп | 2 | |
Другие медикаменты / не принимает медикаменты | 1 | |
| Диагностика | ||
Низкий риск (Н) | Профилактические меры сестринского ухода | 7–11 |
Высокий риск | Меры для пациентов высокого риска падения | 12–23 |
После выявления высокого риска падения, а вероятнее всего, развития саркопении следует обучить пациента
и лиц по уходу по предотвращению падения:
– вставать не спеша: не вставать с постели/стула одному, не вставать резко (если кружится голова, после
анестезии/операции/родов, после принятия лекарственных средств);
– звать на помощь ухаживающее лицо или вызвать медперсонал по кнопке вызова, если нужно в туалет
/ другое;
– для детей по возможности использовать коляску/кювез;
– носить нескользкую обувь (носки, невысокие каблуки).
В отделении стационара или поликлиники:
– должен быть чистый сухой пол, а медперсонал должен убирать с пути преграды (шнуры, провода);
– пациент должен попросить немедленно вытереть мокрое место на полу, обращать внимание на знак «Осторожно, мокрый пол!»
При низком риске падения
необходимо:
– установить высоту кровати на нижнем положении;
– закрепить кроватные колеса, ходунки, инвалидное кресло в устойчивом положении;
– поставить коляску и другие вспомогательные предметы рядом с пациентом;
– обеспечить хорошее освещение;
– сообщить техотделам о неисправностях (например, если не работает кнопка вызова);
– напомнить, чтобы пациент носил нескользкую обувь;
– при сопровождении пациента сообщить персоналу другого отделения о саркопении у пациента.
Если высокий риск (51 балл
и выше у взрослых, 12 и выше у детей):
– на браслет пациента наклеить полоску красного цвета (не закрывая текст) или надеть браслет красного
цвета (при наличии);
– наклеить соответствующий знак снаружи палаты: на входной двери палаты у взрослых установить знак «красный
квадрат»;
– на входной двери палаты у детей установить знак Хампти-Дампти;
– провести дополнительное обучение пациента / лица по уходу;
– совершать обходы в палату каждые 2 ч, особенно ночью, в моменты пробуждения;
– поднять боковые ограждения / борты койки;
– сопровождать в туалет;
– сопровождать пациента после операции, родов, анестезии, седации, инвазивной процедуры;
– по мере возможности разместить пациента в палате, ближайшей к посту;
– постараться обеспечить присутствие лица по уходу или санитарки;
– ознакомить пациента и (или) лиц по уходу о принимаемых лекарственных средствах, об их влиянии на падение (головокружение, слабость).
Средний медицинский
персонал (постовая сестра/брат) должен завести специальную форму и провести
повторную оценку риска падения по шкале Морзе (табл. 2) для взрослых и по шкале «Хампти-Дампти» для детей [24].
Таблица 2.
Шкала Морзе [24]
Параметр | Критерий | Баллы |
Падал ли в последние 3 месяца | Да | 25 |
Нет | 0 | |
Сопутствующие заболевания | Да | 15 |
Нет | 0 | |
Способность ходить | Ходит самостоятельно | 0 |
Ходит сам, с помощью кого-то или строгий постельный режим, неподвижный | 15 | |
Ходит с костылями, ходунками, тростью, опирается о мебель или стены для поддержки | 30 | |
В лечении парентеральное введение средств (гепарин и т. д.) | Да | 20 |
Нет | 0 | |
Походка | Нормальная, ходит свободно | 0 |
Слегка несвободная походка, ходит с остановками, шаги короткие, иногда с задержкой | 10 | |
Нарушения: не может встать, ходит опираясь, смотрит вниз | 20 | |
Психическое состояние | Знает свою способность двигаться | 0 |
Не знает или забывает, что нужна помощь при движении | 15 | |
| Оценка результата | ||
Нет риска | Основной уход | 0–24 |
Низкий риск падения | Профилактические меры | 25–50 |
Высокий риск падения | Принимать меры для пациентов высокого риска падения, оценивать повторно | 51 и более |
Экспертами EWGSOP2 для диагностики саркопении предложено
скрининговое уравнение Ishii, основанное на трех переменных: возрасте, силе
захвата (измеренной динамометром) и окружности голени. Можно использовать тест
на вставании со стула для оценки показателя силы мышц ног. Вариантов его
проведения два. Можно определить временной интервал для пятикратного подъема из
сидячего положения со стула без использования рук или другой вариант: сколько
раз пациент может подняться и сесть на стул за 30-секундный интервал. У
подростков используют те же тесты, что и у взрослых [1].
Золотого стандарта оценки
двигательной активности для детей не существует. У детей раннего возраста
отставание в психомоторном развитии по отношению к возрасту может быть признаком
серьезных нарушений моторики, а не только косвенным признаком наличия
саркопении. Существуют таблицы моторной активности и развития мелкой моторики
детей в зависимости от возраста, на которые ориентируются как педиатры, так и
педагоги. С 2 до 12 лет зарубежные авторы предлагают использовать ряд тестов:
– тест общего моторного развития TGMD-2 (Test of Gross Motor Development) – единственный инструмент,
который оценивает общие моторные навыки изолированно и фокусируется на качестве
выполнения [25];
– для детей с ДЦП есть специализированный тест для оценки больших моторных функций GMFCS (Gross Motor Function Classification System), где дети с уровнем I мало отличаются от типично развивающихся детей, а с уровнем V нуждаются
в уходе [26, 27];
– уровень развития мелкой моторики у детей с ДЦП определяют по шкале нарушения функции рук MACS (Manual
Ability Classification System for children with Cerebral Palsy) [26, 27].
Другие оценки общей
моторики проводятся в сочетании с оценкой мелкой моторики и (или) равновесия (табл. 3):
– MAND (оценка
нервно-мышечного развития Маккэррона);
– MABC-2 (батарея оценки движения для детей);
– BOT-2 (тест Брюнинкса – Озерецкого на моторные навыки);
– PDMS-2 (моторные шкалы развития Пибоди).
Либо как компонент оценки развития:
– NSMDA (критерии оценки от гиперактивной реакции до ее отсутствия по 8-балльной системе от +4 до –4),
– Bayley-III (шкала Бейли-III развития младенцев и малышей).
Несмотря на вариативность
структуры тестов, все они оценивают передвижение детей с включением оценки
ходьбы, бега или подъема по лестнице, бросание и ловлю меча, задачи
статического или динамического равновесия (прыжки или стояние на одной ноге) в
возрастном аспекте [25]. Эти доступные тесты различаются по
простоте использования и интерпретируемости в клинических и исследовательских задачах
с отсылкой к нормам или их критериям.
Таблица 3. Инструменты оценки общей моторики [25]
Тест | Проверяемые навыки | Основные компоненты тестирования | Возрастной диапазон | Диагностические критерии |
Bayley-III | Общая и мелкая моторика, когнитивная, коммуникативная, социальная/эмоциональная, адаптивная | Статические позы, динамические движения, равновесие | От 1 мес. до 3 лет | Задержки развития оценивается ниже 25 перцентиля или ниже 2 SD |
ВОТ-2 | Общая и мелкая моторика | Координация, равновесие, скорость и ловкость бега, сила | 4–21 год | Сравнение с нормами развития |
МАВС-2 | Общая и мелкая моторика, равновесие | Прицеливание и ловля, статистический и динамический баланс | 3–16 лет | Система светофоров: зеленый – норма, желтый – группа риска, красный – нарушение двигательной активности более 15% |
МАND | Общая и мелкая моторика | Координация, прыжки, статическое и динамическое равновесие | 3–25 лет | NDI 70–85 – легкая, 55–69 – умеренная, менее 55 – тяжелая инвалидность |
NSMDA | Общая и мелкая моторика, неврологическое, постуральное, сенсомоторное развитие, модели движения у младенцев | Сидение, стояние на коленях, ходьба, равновесие, бег, прыжки, подтягивание, планирование движений | От 1 мес. до 6 лет | Общий балл 6–8 – нормальный, 9–11 – минимальный, 12–14 – легкая, 15–19 – умеренная, 20–25 – тяжелая, более 25 – глубокая инвалидизация |
PDMS-2 | Общая и мелкая моторика | Неподвижность (равновесие в положении стоя, приседания, отжимания), локомоция (ходьба, бег, прыжки, подскакивание и т. д.), манипулирование объектами (удар ногой, бросок, попадание, ловля) | От рождения до 5 лет | Сравнение с нормами развития |
TGMD-2 | Общая моторика | Локомоция (бег, галоп, подскок, подскакивание, скольжение) и контроль объекта (отбивание, дриблинг, ловля, удар ногой, бросок) | 3–10 лет | Сравнение с нормами развития |
Инструментальная диагностика саркопении
Объективно саркопению
можно диагностировать при углубленной оценке нутритивного статуса с
использованием двухэнергетической рентгеновской абсорбциометрии (Dual-Energy X-ray
Absorptiometry – DEXA), компьютерной, магнитно-резонансной томографии или на
менее инвазивных методов – биоимпедансометрии и ультразвуковой диагностики с
определенной степенью градации эхогенности мышц по J.Z. Heckmatt et al. [1, 4, 6, 28–31]. Во всех случаях соотношение долей мышечной и жировой
массы будет в пользу жировой массы по отношению к нормам распределения этих
тканей в организме.
Количественная оценка
мышечной и жировой массы может быть оценена с помощью биоимпедансометрии. Этот
неинвазивный и простой метод позволяет оценить доли этих тканей в компонентном
составе тела, а также активность мышечной ткани посредством оценки доли
активной клеточной массы. Способ диагностики саркопении, основанный на оценке
компонентного состава тела методом биоимпедансометрии, предложен авторами из
Санкт-Петербурга. Отличается от предложенных ранее DEXA, компьютерной или
магнитно-резонансной томографии тем, что определяет долю объема жировой и
активной клеточной ткани в компонентном составе организма: при сочетании доли жировой
массы 40,5% и выше и доли активной клеточной массы 37% и ниже диагностируют
саркопению, а при сочетании доли жировой массы 30,5% и выше и доли активной клеточной
массы от 37 до 43,5% диагностируют пресаркопению [32].
Возможна
молекулярно-генетическая диагностика саркопении [33],
предрасположенности к ней и вариативности ее клинических фенотипов [34–36]. Влияет на развитие саркопении
исходный пул половых гормонов [37], микробиом кишечника через ось «микробиом
– мышцы» [38]. Тяжесть саркопении определяют в
зависимости от функциональной активности мышц.
Возможности профилактики
и коррекции саркопении
Возможные способы профилактики
и коррекции саркопении предложили А.В. Николайчук и др. через изменение
микробиоты кишечника [39]. Специалисты Л. Стенман и С.
Лахтинен использовали бифидобактерии и несколько пребиотиков и (или) пищевых
волокон для увеличения безжировой массы тела у млекопитающих [40]. Однако без адекватного белкового
обеспечения организма любые медикаментозные или биологически активные вещества
и добавки бессильны. Мышцы являются крупнейшим резервуаром белка в организме,
при этом мышечные белки заменяются со скоростью 1–2% в день. Рекомендации по питанию при саркопении в основном
касаются учета адекватного потребления белка и адекватного статуса витамина D.
Учитывая роль недостаточного питания в патофизиологии саркопении, адекватное
потребление энергии важно для предотвращения потери мышечной массы [41–43]. Необходимо отметить, что только
пищевое сопровождение пациента с саркопенией не эффективно без регулярных
физических нагрузок.
Мультидисциплинарный
подход к работе с пациентом с саркопенией на фоне лечения основного заболевания
включает в себя полноценное питание (адекватное субстратное обеспечение с
коррекцией по микронутриентам), восстановление микрофлоры кишечника и
двигательной активности пациента. Состав мультидисциплинарной команды и возможные
роли представлены на рис. 3.
Рисунок
3. Мультидисциплинарный подход к лечению саркопении у
детей
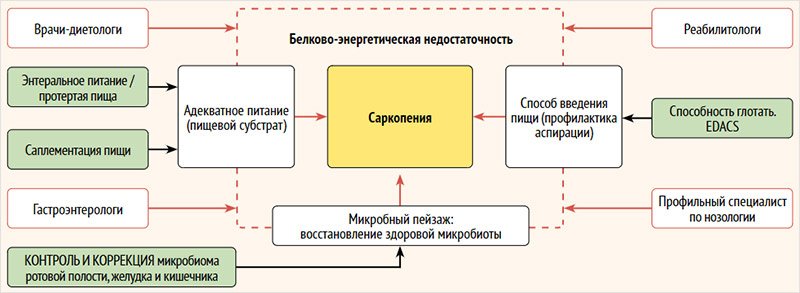
EDACS (Eating and Drinking Ability Classification System) – система классификации способности принятия пищи и жидкости
Заключение
Нелеченная саркопения
повышает риск переломов, ухудшает способность к выполнению деятельности в
повседневной жизни, ассоциируется с сердечно-сосудистыми и респираторными
заболеваниями, когнитивными нарушениями, способствует снижению качества жизни,
возможности самостоятельного передвижения или необходимости длительного
размещения в отделениях сестринского ухода или хосписах и дорого обходится
системам здравоохранения, поскольку сопряжена с личными, социальными и
экономическими трудностями.
Список литературы / References
- Cruz-Jentoft AJ, Bahat G, Bauer J, Boirie Y, Bruyère O, Cederholm T et al. Sarcopenia: revised European consensus on definition and diagnosis. Age Ageing. 2019;48(1):16-31. https://doi.org/10.1093/ageing/afy169.
- Nishikawa H, Fukunishi S, Asai A, Yokohama K, Nishiguchi S, Higuchi K. Pathophysiology and mechanisms of primary sarcopenia (Review). Int J Mol Med. 2021;48(2):156. https://doi.org/10.3892/ijmm.2021.4989.
- Cruz-Jentoft AJ, Baeyens JP, Bauer JM, Boirie Y, Cederholm T, Landi F et al. Sarcopenia: European consensus on definition and diagnosis: Report of the European Working Group on Sarcopenia in Older People. Age Ageing. 2010;39(4):412-423. https://doi.org/10.1093/ageing/afq034.
- Григорьева ИИ, Раскина ТА, Летаева МВ, Малышенко ОС, Аверкиева ЮВ, Масенко ВЛ, Коков АН. Саркопения: особенности патогенеза и диагностики. Фундаментальная и клиническая медицина. 2019;4(4):105-116. https://doi.org/10.23946/2500-0764-2019-4-4-105-116.
- Хорошилов ИЕ. Саркопения у больных: возможности диагностики и перспективы лечения. Лечащий врач. 2017;(8):36-40. Режим доступа: https://www.lvrach.ru/2017/08/15436784.
- Завьялова АН, Хавкин АИ, Новикова ВП. Причины и варианты профилактики саркопении у детей. Российский вестник перинатологии и педиатрии. 2022;67(2):34-42. https://doi.org/10.21508/1027-4065-2022-67-2-34-42.
- Завьялова АН, Трошкина МЕ, Щербак ЛА, Новикова ВП. Саркопеническое ожирение у детей. Экспериментальная и клиническая гастроэнтерология. 2023;(1):134-141. https://doi.org/10.31146/1682-8658-ecg-209-1-134-141.
- Safer U, Kaplan M, Binay Safer V. Evaluation of Sarcopenia in Children. J Surg Res. 2019;237:112. https://doi.org/10.1016/j.jss.2018.03.008.
- Гречаный СВ, Гузева ВИ, Иванов ДО (ред.). Руководство по педиатрии. Т. 9. Неврология и психиатрия детского возраста. СПб.: СПбГПМУ; 2021. 288 с.
- Клочкова ОА, Куренков АЛ. Мышечная слабость и утрата двигательных навыков у пациентов с детским церебральным параличом. Вопросы современной педиатрии. 2020;19(2):107-115. https://doi.org/10.15690/vsp.v19i2.2103.
- Иванов ДО, Завьялова АН, Новикова ВП, Гавщук МВ, Яковлева МН, Кликунова КА. Влияние пищевого субстрата и способа кормления на компонентный состав тела у пациентов с церебральным параличом. Профилактическая и клиническая медицина. 2022;84(3):15-27. https://doi.org/10.47843/2074-9120_2022_3_15.
- Jeon I, Bang MS, Lim JY, Shin HI, Leigh JH, Kim K et al. Sarcopenia among Adults with Cerebral Palsy in South Korea. PM R. 2019;11(12):1296-1301. https://doi.org/10.1002/pmrj.12134.
- Peterson MD, Gordon PM, Hurvitz EA. Chronic disease risk among adults with cerebral palsy: the role of premature sarcopoenia, obesity and sedentary behaviour. Obes Rev. 2013;14(2):171-182. https://doi.org/10.1111/j.1467-789X.2012.01052.x.
- Сабиров ИС, Кожоева МЗ, Ибадуллаев БМ, Мадаминов ЖБ, Абдыманап кызы А. Саркопения и новая короновирусная инфекция (COVID-19). The Scientific Heritage. 2021;(63-2):39-46. https://doi.org/10.24412/9215-0365-2021-63-2-39-46. Sabirov IS, Kozhoeva MZ, Ibadullaev BM, Madaminov ZhB, Abdymanap kyzy A. Sarcopenia and new coronavirus infection (COVID-19). The Scientific Heritage. 2021;(63-2):39-46. (In Russ.) https://doi.org/10.24412/9215-0365-202163-2-39-46.
- Jensen GL. Inflammation: roles in aging and sarcopenia. JPEN J Parenter Enteral Nutr. 2008;32(6):656-659. https://doi.org/10.1177/0148607108324585.
- Abiri B, Vafa M. Nutrition and sarcopenia: A review of the evidence of nutritional influences. Crit Rev Food Sci Nutr. 2019;59(9):1456-1466. https://doi.org/10.1080/10408398.2017.1412940.
- Nishikawa H, Fukunishi S, Asai A, Yokohama K, Nishiguchi S, Higuchi K. Pathophysiology and mechanisms of primary sarcopenia (Review). Int J Mol Med. 2021;48(2):156. https://doi.org/10.3892/ijmm.2021.4989.
- Завьялова АН, Новикова ВП, Игнатова ПД. Ось «микробиота - мышцы». Экспериментальная и клиническая гастроэнтерология. 2022;(11):60-69. https://doi.org/10.31146/1682-8658-ecg-207-11-60-69.
- Lang T, Streeper T, Cawthon P, Baldwin K, Taaffe DR, Harris TB. Sarcopenia: etiology, clinical consequences, intervention, and assessment. Osteoporos Int. 2010;21(4):543-559. https://doi.org/10.1007/s00198-009-1059-y.
- Polyzos SA, Mathew H, Mantzoros CS. Irisin: A true, circulating hormone. Metabolism. 2015;64(12):1611-1618. https://doi.org/10.1016/j.metabol.2015.09.001.
- Bergen HR 3rd, Farr JN, Vanderboom PM, Atkinson EJ, White TA, Singh RJ et al. Myostatin as a mediator of sarcopenia versus homeostatic regulator of muscle mass: insights using a new mass spectrometry-based assay. Skelet Muscle. 2015;5:21. https://doi.org/10.1186/s13395-015-0047-5.
- Цориев ТТ, Белая ЖЕ, Рожинская ЛЯ, Мельниченко ГА, Гребенникова ТА, Ильин АВ и др. Содержание миокинов в сыворотке крови у пациентов с эндогенным гиперкортицизмом и акромегалией: одномоментное исследование «случай - контроль». Вестник Российской академии медицинских наук. 2016;71(3):9-14. https://doi.org/10.15690/vramn659.
- Chang JS, Kim TH, Nguyen TT, Park KS, Kim N, Kong ID. Circulating irisin levels as a predictive biomarker for sarcopenia: A cross-s ectional community-based study. Geriatr Gerontol Int. 2017;17(11):2266-2273. https://doi.org/10.1111/ggi.13030.
- Kim EJ, Lim JY, Kim GM, Min J. An electronic medical record-based fall risk assessment tool for pediatric inpatients in South Korea: Improved sensitivity and specificity. Child Health Nurs Res. 2021;27(2):137-145. https://doi.org/10.4094/chnr.2021.27.2.137.
- Griffiths A, Toovey R, Morgan PE, Spittle AJ. Psychometric properties of gross motor assessment tools for children: a systematic review. BMJ Open. 2018;8(10):e021734. https://doi.org/10.1136/bmjopen-2018-021734.
- Строкова ТВ, Камалова АА, Завьялова АН, Таран НН, Иванов ДО, Александрович ЮС и др. Принципы нутритивной поддержки у детей с детским церебральным параличом. В: Бельмер СВ, Ильенко ЛИ (ред.). Актуальные проблемы абдоминальной патологии у детей: материалы ХХVIII Конгресса детских гастроэнтерологов России и стран СНГ, Москва, 23-25 марта 2021 г. М.: МЕДПРАКТИКА-М; 2020. С. 290-335.
- Иванов ДО, Строкова ТВ, Камалова АА, Александрович ЮС, Таран НН, Завьялова АН и др. Диагностика и коррекция нутритивного статуса у детей с детским церебральным параличом. СПб.: Санкт-П етербургский государственный педиатрический медицинский университет; 2020. 100 с.
- Барбараш ОЛ, Коков АН, Масенко ВЛ, Кареева АИ. Способ определения саркопении с использованием количественной оценки мышечной ткани по данным компьютерной томографии грудной клетки. Патент RU 2754291C1, 31.08.2021. Режим доступа: https://yandex.ru/patents/doc/RU2754291C1_20210831.
- Закревский АИ, Фёдорова АА, Пасечник ИН, Кутепов ДЕ. Саркопения: как ее диагностировать? Клиническое питание и метаболизм. 2021;2(1):13-22. https://doi.org/10.17816/clinutr71107.
- Metzger GA, Sebastião YV, Carsel AC, Nishimura L, Fisher JG, Deans KJ, Minneci PC. Establishing Reference Values for Lean Muscle Mass in the Pediatric Patient. J Pediatr Gastroenterol Nutr. 2021;72(2):316-323. https://doi.org/10.1097/MPG.0000000000002958.
- Gilligan LA, Towbin AJ, Dillman JR, Somasundaram E, Trout AT. Quantification of skeletal muscle mass: sarcopenia as a marker of overall health in children and adults. Pediatr Radiol. 2020;50(4):455-464. https://doi.org/10.1007/s00247-019-04562-7.
- Завьялова АН, Новикова ВП, Кликунова КС, Гавщук МВ, Лисовский ОВ. Способ диагностики саркопении. Евразийский патент на изобретение №044862, 06.10.2023. Режим доступа: https://old.eapo.org/ru/patents/reestr/patent.php?id=44862.
- Кучер АН. Молекулярно-генетические маркеры саркопении. Молекулярная медицина. 2021;19(1):17-29. https://doi.org/10.29296/24999490-2021-01-03.
- Sgrò P, Sansone M, Sansone A, Sabatini S, Borrione P, Romanelli F, Di Luigi L. Physical exercise, nutrition and hormones: three pillars to fight sarcopenia. Aging Male. 2019;22(2):75-88. https://doi.org/10.1080/13685538.2018.1439004.
- Tan LJ, Liu SL, Lei SF, Papasian CJ, Deng HW. Molecular genetic studies of gene identification for sarcopenia. Hum Genet. 2012;131(1):1-31. https://doi.org/10.1007/s00439-011-1040-7.
- Korostishevsky M, Steves CJ, Malkin I, Spector T, Williams FM, Livshits G. Genomics and metabolomics of muscular mass in a community-b ased sample of UK females. Eur J Hum Genet. 2016;24(2):277-283. https://doi.org/10.1038/ejhg.2015.85.
- Мокрышева НГ, Крупинова ЮА, Володичева ВЛ, Мирная СС, Мельниченко ГА. Саркопения глазами эндокринолога. Ожирение и метаболизм. 2018;15(3):21-27. https://doi.org/10.14341/omet9792.
- Тюзиков ИА, Калинченко СЮ. Саркопения: помогут ли только протеиновое питание и физическая активность? Роль половых стероидных гормонов в механизмах регуляции синтеза мышечного белка. Вопросы диетологии. 2017;7(2):41-50. https://doi.org/10.20953/2224-5448-2017-2-41-50.
- Николайчук АВ, Соколова АВ, Драгунов ДО, Тихомирова МА, Дуванов ИА. Изменение микробиоты кишечника и риск прогрессирования саркопении. Лечебное дело. 2020;(1):18-22. https://doi.org/10.24411/2071-53152020-12188.
- Стенман Л, Лахтинен С. Бифидобактерии для увеличения безжировой массы тела. Патент RU 2757213C2, 12.10.2021. Режим доступа: https://yandex.ru/patents/doc/RU2757213C2_20211012.
- Voisin S, Jacques M, Landen S, Harvey NR, Haupt LM, Griffiths LR et al. Meta-analysis of genome-wide DNA methylation and integrative omics of age in human skeletal muscle. J Cachexia Sarcopenia Muscle. 2021;12(4):1064-1078. https://doi.org/10.1002/jcsm.12741.
- Завьялова АН, Новикова ВП, Кликунова КА. Юношеская саркопения у пациентов с детским церебральным параличом и предикторы ее развития. Forcipe. 2022;5(S2):207-208. Режим доступа: https://ojs3.gpmu.org/index.php/forcipe/article/view/4479.
- Davis JA, Mohebbi M, Collier F, Loughman A, Staudacher H, Shivappa N et al. The role of diet quality and dietary patterns in predicting muscle mass and function in men over a 15-year period. Osteoporos Int. 2021;32(11):2193-2203. https://doi.org/10.1007/s00198-021-06012-3.



 1
1 2
2 3
3 4
4


Комментарии (0)