Фото: Fantastic Studio/FOTODOM/Shutterstoсk
Журнал "Медицинский совет" №23/2025
DOI: 10.21518/ms2025-529
М.Д. Ардатская, https://orcid.org/0000-0001-8150-307X
И.В. Зверков, https://orcid.org/0000-0001-6210-8955
Л.В. Масловский, https://orcid.org/0000-0002-5111-8127
Т.Б. Топчий, https://orcid.org/0000-0003-4491-881X
О.Н. Минушкин, https://orcid.org/0000-0002-7723-7992
Центральная государственная медицинская академия Управления делами Президента РФ; 121359, Россия, Москва, ул. Маршала Тимошенко, д. 19, стр. 1а
Состояние кишечной микробиоты во многом определяет течение патологических процессов в организме человека. В настоящее время не вызывает сомнений роль дисбиоза в развитии и прогрессировании многих расстройств, включая кишечные инфекции, СРК (синдром раздраженного кишечника), ВЗК (воспалительные заболевания кишечника), СИБР (синдром избыточного роста бактерий), дивертикулярную болезнь, целиакию, рак, непереносимость пищи, аллергию, заболевания печени и поджелудочной железы, ожирение, диабет, метаболический синдром, гематологические, кардиологические, мочеполовые, ревматологические, неврологические и нейропсихиатрические. Разработка средств, корректирующих нарушения баланса микробиоты кишечника, является одним из самых перспективных направлений современной науки. Совершенствуются и методы диагностики нарушений кишечной микробиоты. Важность и целесообразность включения средств, модулирующих состояние кишечной микробиоты, в состав комплексной терапии многих заболеваний подтверждается многочисленными зарубежными и отечественными исследованиями. Эволюция пробиотических средств прошла путь от монокомпонентных препаратов, содержащих один штамм микроорганизмов, до современных многоштаммовых синбиотических комплексов, сочетающих пробиотики и пребиотики. Первые поколения пробиотиков были направлены преимущественно на восполнение дефицита полезных бактерий, в то время как современные биокомплексы обладают многоуровневым действием – они регулируют состав и активность микробиоценоза, способствуют синтезу короткоцепочечных жирных кислот и других необходимых низкомолекулярных метаболитов бактериального происхождения, улучшают барьерную функцию кишечника и модулируют иммунный ответ организма. Настоящая обзорная статья посвящена оценке эффективности синбиотических биокомплексов Нормофлорин Л, Б, Д в коррекции нарушений кишечного микробиоценоза при антибактериальной терапии, функциональных заболеваниях кишечника, воспалительных заболеваниях кишечника, хронических панкреатитах, целиакии, метаболических расстройствах и ожирении, заболеваниях лор-органов, дерматологических и гинекологических заболеваниях.
Для цитирования: Цуканов ВВ, Черепнин МА, Тонких ЮЛ, Васютин АВ. Эффективность комбинированной терапии мебеверином и псиллиумом у пациентов с синдромом раздраженного кишечника с преобладанием запора. Медицинский совет. 2025;19(15): https://doi.org/10.21518/ms2025-344
Конфликт интересов: авторы заявляет об отсутствии конфликта интересов.
Effectiveness of synbiotic biocomplexes in correction of gut microbiocenosis disorders
Maria D. Ardatskaya, https://orcid.org/0000-0001-8150-307X
Igor V. Zverkov, https://orcid.org/0000-0001-6210-8955
Leonid V. Maslovskii, https://orcid.org/0000-0002-5111-8127
Tatyana B. Topchiy, https://orcid.org/0000-0003-4491-881X
Oleg N. Minushkin, https://orcid.org/0000-0002-7723-7992
Central State Medical Academy of Department for Presidential Affairs of the Russian Federation; 19, Bldg. 1а, Marshal Timoshenko St., Moscow, 121359, Russia
The state of
the gut microbiota largely determines the course of pathological processes in
the human body. Currently, there is no doubt about the role of dysbiosis in the
development and progression of many disorders, including intestinal infections,
IBS, IBD, SIBO, diverticular disease, celiac disease, cancer, food intolerance,
allergies, liver and pancreatic diseases, obesity, diabetes, metabolic
syndrome, hematological, cardiological, genitourinary, rheumatological,
neurological and neuropsychiatric. The development of tools that correct the
imbalance of the gut microbiota is one of the most promising areas of the
modern science. Methods for diagnosing disorders of the gut microbiota are also
being improved. The importance and expediency of including agents that modulate
the state of the gut microbiota in the complex therapy of many diseases is
confirmed by numerous foreign and domestic studies. The evolution of probiotic
products has progressed from single-strain formulations containing one type of
microorganism to modern multi-strain synbiotic complexes that combine
probiotics and prebiotics. The first generations of probiotics were primarily
aimed at replenishing beneficial bacteria, whereas contemporary biocomplexes
exert multi-level effects — they regulate the composition and activity of the
gut microbiocenosis, promote the synthesis of necessary bacterial metabolites,
improve intestinal barrier function, and modulate the immune response. This
review article is devoted to evaluating the effectiveness of synbiotic
biocomplexes Normoflorin L, B, and Д in the correction of gut microbiocenosis disorders in
antibacterial therapy, functional bowel diseases, inflammatory bowel diseases,
chronic pancreatitis, celiac disease, metabolic disorders and obesity, diseases
of the ENT organs, dermatological and gynecological diseases.
For citation: Tsukanov VV, Cherepnin MA, Tonkikh JuL, Vasyutin AV. Efficiency of combination therapy with mebeverine and psyllium in patients with irritable bowel syndrome with predominant constipation. Meditsinskiy Sovet. 2025;19(15): https://doi.org/10.21518/ms2025-344
Conflict of interest: the authors declares no conflict of interest.
Введение
В настоящее время не вызывает сомнений
патогенетическая роль нарушений кишечного микробиоценоза в развитии и, что еще
более важно, прогрессировании функциональных заболеваний желудочно-кишечного
тракта (ЖКТ), метаболических расстройств, болезней сердца, астмы и рассеянного
склероза, а также при неврологических состояниях, таких как аутизм. И спектр
патологий, ассоциированных с дисбиозом и повышенной проницаемостью кишечного
барьера, постоянно расширяется.
Результаты проведенных нами исследований
позволяют констатировать, что у 100% больных с патологией ЖКТ и других органов
и систем диагностируются изменения со стороны микрофлоры и ее активности [1–6].
Широкий спектр современных средств,
применяемых для восстановления численности, качественного состава и метаболической
активности кишечной микробиоты представлен разнообразными микроэкологическими
лекарственными препаратами, биологическими пищевыми добавками и продуктами
функционального питания [7–9]. Эволюция средств, модулирующих кишечную
микробиоту, представлена на рис. 1.
Рисунок
1. Эволюция препаратов, влияющих на микрофлору
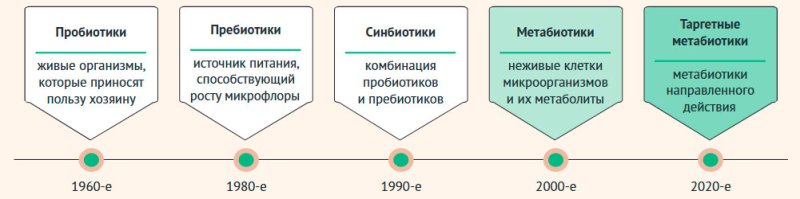
Эволюция
пробиотических препаратов
Пробиотики – самая многочисленная и
наиболее изученная группа веществ, модулирующих кишечную микробиоту. Термин
«пробиотик» применяется в отношении живых микроорганизмов и продуктов их
ферментации, обладающих антагонистической активностью по отношению к патогенной
микрофлоре и оказывающих оздоровительное действие на организм человека, доказанное в
контролируемых клинических исследованиях на человеке. К таким микроорганизмам
относятся различные виды лактобактерий (Lactobacillus acidophilus, L.
casei, L. delbrueckii subsp. bulgaricus), бифидобактерий (B.
bifidum, B. breve, B. longum, B. infanris, B.
animalis), термофильный (молочный) стрептококк, сахаромицеты, некоторые
штаммы сенной палочки (Bacillus subtilis).
К пробиотическим лекарственным препаратам предъявляются
строгие требования:
- соответствие штаммового состава задачам
восстановления нормальной иерархической структуры доминирования видов, т. е.
наличие в составе бифидо- и лактобактерий;
- сохранение жизнеспособности бактерий при
прохождении через ЖКТ, их устойчивость к действию желчных кислот, соляной
кислоты и панкреатических ферментов (это свойство может быть определено заранее
in vitro);
- способность к адгезии к эпителию
слизистой оболочки кишечника;
- возможность колонизации кишечника или
соответствующего органа-мишени;
- способность синтезировать антимикробные
вещества, активные против патогенных микроорганизмов;
- безопасность при применении у человека:
штамм, входящий в состав препарата, должен быть зарегистрирован в международном
депозитарии штаммов согласно номенклатуре;
- количество бактериальных клеток в
капсуле или таблетке на момент продажи должно быть не менее миллиарда (109)
и способствовать уничтожению патогенных микроорганизмов в кишечнике, не
оказывая при этом отрицательного влияния на другие полезные бактерии;
- стабильность при хранении в обычных
условиях;
- клинически доказанная польза для
здоровья [10, 11].
Эффекты, оказываемые пробиотиками на
здоровье человека, реализуются в трех основных направлениях:
1) эффекты общего характера:
-
синтез нутриентов и антиоксидантов;
-
активация MALT-системы;
-
модуляция ответа Th1/Th2;
-
контроль потенциально патогенных микробов;
-
снижение продукции эндотоксинов;
-
снижение мутагенности;
2) гуморальные эффекты:
-
ингибирование синтеза IgE;
-
стимуляция продукции IgA;
-
симуляция выработки NO;
-
модулирование цитокинового ответа;
3) клеточные эффекты:
-
стимуляция работы макрофагов;
-
способствование росту и регенерации клеток;
-
способствование физиологическому апоптозу [12].
В медицинской практике пробиотические
препараты представлены 5 поколениями:
1) монокомпонентные
препараты, содержащие 1 штамм бактерий;
2) пробиотики,
основанные на использовании неспецифических для человека микроорганизмов и
являющиеся самоэлиминирующимися антагонистами;
3) поликомпонентные
препараты, в состав которых входят несколько симбиотических штаммов бактерий;
4) иммобилизованные
на сорбенте бифидосодержащие препараты;
5) препараты
адресного действия, специализированные пробиотики с узкими показаниями к
применению.
Благодаря десятилетиями накопленной
научной базе концепция длительной заместительной колонизации пробиотиками
кишечника человека уступила место признанию транзиторности нахождения
пробиотических организмов в кишечнике. Однако, несмотря на статус проходной
флоры, современные пробиотические продукты в составе программ терапии различных
заболеваний преследуют решение следующих задач [1] [13–15]:
- селективная стимуляция иммунной системы;
- воздействие на ключевое звено (звенья)
патогенеза заболевания (токсины, адгезию, инвазию, транслокацию);
- влияние на отдельный механизм действия
основного лекарственного препарата (например, улучшение антимикробного эффекта
антибиотиков);
- дополнение эффектов основного препарата
(например, гиполипидемических средств, антигистаминных препаратов, регуляторов
моторики и т. д.);
- «переключение» ответа макроорганизма на
воздействие патогенетического фактора (например, при иммуносупрессии, ВЗК);
- профилактика реинфекции.
При выборе препарата и тактики
использования пробиотиков необходимо учитывать ряд факторов:
- особенности и потребности возрастных
этапов формирования видового состава кишечного микробиоценоза; - штаммспецифичность: конкретное заболевание
требует применения определенного пробиотического штамма, который имеет
доказанную эффективность именно при данной нозологии; - безопасность: хотя в целом пробиотики
считаются безопасными, и это подтверждено результатами клинических
исследований, имеется ряд сообщений о нежелательных эффектах, в связи с чем
пробиотические средства не рекомендуются некоторым категориям пациентов:
находящимся в тяжелом состоянии в стационаре; при иммунодефицитных состояниях;
при недоношенности; при наличии синдрома КК; при поражениях клапанного аппарата
сердца; - форма выпуска и суточная доза.
Все вышеизложенное приглашает к
дальнейшему поиску и расширению возможностей использования пробиотиков,
учитывая их многофункциональность, в схемах лечения различной патологии
желудочно-кишечного тракта (ЖКТ).
Цель настоящего обзора — оценить
клиническую эффективность биокомплексов Нормофлорин Л, Б, Д в составе терапии
различных заболеваний.
Клиническое
применение биокомплексов Нормофлорин
Биокомплексы Нормофлорин Л, Б, Д — жидкие
комбинированные пробиотики (синбиотики), эффективность которых обеспечивается
трехкомпонентным составом: пробиотиками, бактериальными метаболитами (органические
кислоты, бактериоцины, лизоцим, витамины, микроэлементы и минералы,
аминокислоты, мурамилдипептид, ферменты) и пребиотиком лактитол. Пробиотики в
составе Нормофлорина живые, физиологически активные.
Жидкие формы пробиотиков обладают целым
рядом преимуществ:
- активны с первых минут контакта со
слизистой;
- реальная концентрация 1010
живых бактерий в 1 мл препарата;
- 100% популяций бактерий увеличивается в
процессе производства;
- более 90% бактерий и их метаболитов
осуществляют свой лечебный эффект.
Активными компонентами, входящими в состав
Нормофлорина, являются органические кислоты: молочная, янтарная и короткоцепочечные
жирные кислоты (КЖК). КЖК оказывают многофакторное влияние на физиологию клеток
кишечника (табл. 1).
Таблица 1. Значение короткоцепочечных жирных кислот для организма
Название | Действие на организм |
Молочная | - антимикробный эффект - регулируют уровень РН - выполняют роль «эндогенных слабительных» - регулируют моторную и секреторную активность кишечника |
Уксусная | |
Пропионовая | - регулирует микроциркуляцию в слизистой оболочке и поддерживает в ней трофические процессы - участвует в глюконеогенезе и синтезе биогенных аминов - блокирует адгезию УПМ |
Янтарная | обладает антимикробным и антиоксидантным действием |
Масляная | - является дополнительным автономным источником энергообеспечения кишечного эпителия - участвует в регуляции его дифференцировки и пролиферации |
Содержащиеся в Нормофлорине КЖК
обеспечивают слизистые оболочки дополнительной энергией, способствуют
регенерации поврежденных эпителиальных клеток кишечной стенки, улучшают
трофические процессы слизистой, а также колонизационную резистентность
пищеварительного тракта.
Детоксицирующий эффект Нормофлорина
реализуется за счет подавления транслокации из кишечника в кровь токсических
метаболитов (индола, скатола, биогенных аминов, канцерогенов и т. п.), различного
типа токсинов бактериального происхождения и нейтрализации действия
проканцерогенов. На фоне приема данных биокомплексов повышается уровень естественной
противоинфекционной резистентности за счет стимуляции выработки иммунокомпетентными
клетками организма лизоцима, провоспалительных и противовоспалительных
цитокинов и интерферона.
В состав Нормофлорина не входит молочный
белок и лактоза, поэтому они могут назначаться при наличии у пациента аллергии
к белкам коровьего молока и лактазной недостаточности без возрастных
ограничений.
Эффективность пробиотика L. acidophilus
в составе биокомплекса Нормофлорин Л при антибиотик-ассоциированной диарее
(ААД) доказана по результатам второго метаанализа 9 рандомизированных
клинических исследований (РКИ) [13]. Использовались различные пробиотические
микроорганизмы: дрожжевые грибки (S. boulardii), лактобактерии (L.
acidophilus, L. bulgaricus, L. rhamnosus), штаммы
энтерококков, продуцировавшие молочную кислоту (E. faecium). Оказалось,
что количество случаев диареи, вызванной антибиотиками, было ниже в группе их
применения на 63% по сравнению с плацебо, причем прием дрожжевых грибков снизил
частоту возникновения диареи на 61%.
В состав биокомплекса Нормофлорин Б входят
пробиотики B. bifidum и B. longum. Штамм B. bifidum
эффективен для профилактики некротизирующего энтероколита (НЭК) [16]. Штамм B.
longum в комбинации с L. acidophilus La5 + B. animalis lactis
Bb12; L. helveticus R52 + L. rhamnosus R11; L.
acidophilus nr + E. faecalis nr повышает частоту успешной эрадикации
H.
pylori
[17]. А по результатам другого исследования способствует снижению уровня
холестерина и липопротеинов низкой плотности (ЛПНП) [18].
Биокомплекс Нормофлорин Д содержит L. casei,
B. bifidum, B. longum. В исследовании McFarland показано, что пробиотики
с содержанием L. casei в дозе 107–1010 КОЕ/сут
оказывали превентивное действие на развитие ААД в случае их приема с 1–2-го дня
антибиотикотерапии и далее в течение 1–4 нед. после окончания
антибиотикотерапии [17].
Ряд исследований подтвердил взаимосвязь
между запорами и микробиотой кишечника [19]. Кроме того, во многих клинических
исследованиях выявили, что пробиотики являются эффективными средствами для
облегчения симптомов запора [20].
Роль Lactobacillus (L.
acidophilus, L. rhamnosus, L. reuteri, L. plantarum) и
Bifidobacterium (Bifidobacterium animalis subsp. lactis) была
изучена при запорах в одном из последних крупных исследований. Была доказана
эффективность данных штаммов в борьбе с функциональными запорами [20].
Пробиотики благоприятно влияют на
клинические параметры язвенного колита (UC), болезни Крона (CD) и
некротизирующего энтероколита (NEC) через активацию AhR (рецептор ароматических
углеводородов) метаболитами триптофана (такими как ILA, 5HIAA, IAld и DHNA).
Улучшение симптомов в этих патологиях происходит в основном за счет активации
противовоспалительного ответа, включая повышение экспрессии IL-22 и
генов-мишеней (таких как CYP1A1, NQO1 и Nfr2), а также одновременного снижения
уровня провоспалительных цитокинов TNFα, IL-10 и IL-8. Наиболее часто
используемые микроорганизмы включают Lactobacillus bulgaricus, Streptococcus
thermophilus, Lactobacillus acidophilus, Akkermansia muciniphilia,
Lactiplantibacillus plantarum и различные виды Bifidobacterium [21,
22].
В метаанализе, проведенном Zhao, оценивалось, могут ли пробиотики
устранить последствия иммунотерапии антибиотиками у онкологических больных,
получающих ингибиторы иммунных контрольных точек (ICI). Результаты данного метаанализа
показывают, что использование пробиотиков положительно коррелирует с улучшением
общей выживаемости (OS), выживаемости без прогрессирования заболевания (PFS),
общего уровня ответа (ORR) и контроля над заболеванием (DCR) у пациентов, в
частности, с немелкоклеточным раком легкого (NSCLC). Однако авторы считают
необходимым проведение многоцентровых исследований с большим числом участников,
стандартизированными протоколами лечения и проспективным дизайном для
подтверждения вышеуказанных результатов [23].
В работах российских ученых были также
получены положительные результаты при применении пробиотиков при различных
заболеваниях [12, 24].
Так, применение Нормофлорина Д при
проведении антибактериальной терапии оказалось эффективным для профилактики
дисбиотических нарушений в кишечнике [24]. В исследование включены 30 пациентов
с заболеваниями легких, которые разделены на 2 группы: основная группа 15
человек, которые на фоне проводимой антибактериальной терапии принимали Нормофлорин
Д по 20 мл 2 раза в день в течение 14 дней; контрольная группа 15 человек, в
лечении которых использовались только антибактериальные препараты.
В основной группе после курса коррекции
уменьшились симптомы абдоминальной (от 20 до 7%) и кишечной диспепсии (от 53 до
13%). До лечения изменение характера стула (запор, понос, чередование запоров и
поносов) наблюдалось у 67% пациентов, а после лечения всего у 20% больных,
получивших антибактериальную терапию. В контрольной группе наоборот: если в
начале наблюдения абдоминальная колика беспокоила 13 пациентов, то после
антибактериальной терапии – 20% больных, кишечная диспепсия в начале – 27%
больных, после 60% пациентов жаловались на вздутие живота, метеоризм.
Методом газожидкостного
хроматографического анализа были исследованы КЖК в кале больных исследуемых
групп до и после курсов лечения и у практически здоровых лиц. Исходно у больных
обеих групп наблюдается резкое снижение в 2,5–3 раза абсолютной концентрации
КЖК по сравнению с нормой, снижение доли уксусной и масляной кислот, повышение
доли пропионовой кислоты, что свидетельствует об измененной активности
различных популяций микроорганизмов индигенной толстокишечной микрофлоры.
Значения АИ (анаэробный индекс) отклонены в область резко отрицательных значений.
После проведения антибактериальной терапии
в основной группе отмечается тенденция к повышению абсолютной концентрации КЖК,
происходит формирование нормального профиля кислот: повышение долей уксусной и
масляной кислот при снижении доли пропионовой кислоты, что отражается на
изменении значений АИ, которые смещаются в сторону нормальных значений. В
группе сравнения после лечения происходит дальнейшее увеличение доли
пропионовой кислоты, уксусной кислоты, что свидетельствует об активизации
остаточной микрофлоры и анаэробных микроорганизмов, их микробиологический статус
имел тенденцию к усугублению показателей [24].
Использование Нормофлорина Л и Б в составе
комплексной терапии при синдроме раздраженного кишечника (СРК) обеспечило
положительную динамику клинических проявлений заболевания у 70% больных,
улучшение психологического состояния у них, исчезновение чувства страха,
тревоги, беспокойства [25].
Нормофлорин Л и Б при воспалительных
заболеваниях тонкой кишки как побочном эффекте эрадикационной терапии язвенной
болезни способствовал восстановлению колонизационной резистентности слизистой
кишечника, оптимизации процессов пищеварения, всасывания и детоксикации, улучшению
состояния больных [26]. Также
Е. Еремина и соавт. отмечали, что Нормофлорин Д оказывал благоприятное влияние
на течение язвенной болезни, ассоциированной с H. pylori, способствовал
быстрой нормализации иммунного ответа, тем самым повышая эффективность лечения
[26].
В исследовании И.Д. Лоранской и соавт.
показано, что Нормофлорин Д улучшает самочувствие у больных хроническими
панкреатитами, купирует клинические проявления заболевания, положительно влияет
на общее состояние, улучшает показатели клеточного и гуморального иммунитета [27].
В работе Е. Ткаченко Нормофлорин Д и Л
применялись при хроническом иммуноопосредованном воспалительном заболевании
тонкой кишки у генетически предрасположенных к диарее и стеаторее лиц с
целиакией. По результатам терапии были коррекция клинических показателей,
коррекция дисбиоза кишечника, улучшение показателей качества жизни и
психоэмоциональной сферы [28].
В нашем исследовании 2012 г. оценивалась
клиническая эффективность биокомплексов Нормофлорин Л, Б в лечении
функциональных заболеваний кишечника с синдромом запора. Обследовано 30
пациентов с функциональными заболеваниями кишечника (ФЗК, Римские критерии III,
2006 г.): с синдромом раздраженного кишечника с преобладанием запора — 16
человек, с функциональным запором — 14 человек [29].
Критериями оценки эффективности служили:
динамика клинических симптомов, бактериологическое исследование кала до и после
лечения, время транзита по кишечнику активированного угля — «карболеновая
проба», определение КЖК в кале методом газожидкостной хроматографии до и после
лечения.
На фоне 20-дневного курса лечения
Нормофлорином Л, Б пациенты отмечали положительные сдвиги в клинической
симптоматике. Частота стула нормализовалась у 28 из 30 человек (93,3%), что
позволило им уменьшить дозу слабительных препаратов.
Для оценки состояния микробиоценоза
кишечника мы исследовали содержание и качественный состав КЖК в кале у больных
ФЗК. Результаты проведенных исследований представлены в табл. 2.
Таблица 2. Параметры короткоцепочечных жирных кислот в кале у пациентов с функциональными заболеваниями
кишечника (СРК-З и ФЗ) до и после приема Нормофлорина Л, Б и у практически
здоровых лиц
Группа | Σ (С2 — С6) | Уксусная кислота | Пропионовая кислота | Масляная кислота | АИ | EiCn |
Норма | 10,51 ± 2,25 | 0,634 ± 0,004 | 0,189 ± 0,001 | 0,176 ± 0,004 | — 0,576 ± 0,012 | 0,059 ± 0,009 |
ФЗК (до) | 6,18 ± 1,12 | 0,703 ± 0,002* | 0,153 ± 0,006* | 0,142 ± 0,002* | — 0,419 ± 0,011* | 0,101 ± 0,031* |
ФЗК (после) | 8,91 ± 2,09 | 0,651 ± 0,002** | 0,179 ± 0,006** | 0,170 ± 0,002** | — 0,536 ± 0,011** | 0,077 ± 0,016*,** |
Примечание.
M ± m, для p < 0,05. * р < 0,05 при сравнении с группой нормы. ** р <
0,05 при сравнении показателей до и после лечения.
СРК-3
– синдром раздраженного кишечника с запором, ФЗ – функциональные заболевания, ФЗК
– функциональные заболевания кишечника, АИ – анаэробные индексы
Из табл.
2 видно – исходно у больных с ФЗК с синдромом запора выявлено резкое
увеличение доли уксусной кислоты, являющейся метаболитом не только анаэробной,
но в большей степени аэробной факультативной и остаточной (условно патогенной)
микрофлоры (в частности, родов эшерихий, стрепто-, стафилококков и др.) [30].
Это связано с переключением метаболизма колоноцитов с цикла Кребса на активацию
гексозомонофосфатного шунтирования, что при ФЗК с синдромом запора приводит к
увеличению продукции активных форм кислорода и «аэробизации» среды,
способствующих активизации аэробных микроорганизмов.
Данный факт отражается на изменении
окислительно-восстановительного потенциала как в приэпителиальной зоне, так и в
просвете кишечника и выражается значениями анаэробного индекса (АИ) (И.
Гунзалус, Р. Стайнер, 1963 г.), который смещается в область слабоотрицательных
значений, благоприятных для роста аэробной условно патогенной микрофлоры [30,
31], что соотносится с фактом, описанным выше.
Анализ повышения уровня концентраций
изокислот свидетельствует о возрастании протеолитической активности микрофлоры
за счет увеличения количества слизи в кишечном содержимом. С другой стороны,
изменение данного параметра связано с резкой активизацией аэробных (кишечные
палочки, фекальные стрептококки и стафилококки, некоторые бациллы)
микроорганизмов, представителей факультативной и остаточной (условно
патогенной) микрофлоры, в частности их протеолитических штаммов [30, 31],
которые рассматриваются как сильнейшие протеолитики.
После лечения отмечалось возрастание
абсолютной концентрации КЖК, что свидетельствовало о повышении не только
количества облигатной молочнокислой флоры — бифидо- и лактобактерий (что
согласуется с результатами бактериологического исследования), но и других
представителей резидентной сахаролитической флоры под влиянием содержащихся в
Нормофлорине Л и Б органических кислот, в т. ч. короткоцепочечных, и
пребиотика лактитола (последний подвергается также бактериальной деградации до
КЖК и оказывает слабительное действие — непосредственно осмотическое и за счет
увеличения бактериальной биомассы).
С одной стороны, восстановление продукции
КЖК собственной микрофлорой служит одним из важных маркеров восстановления
механизмов саморегуляции ее роста и жизнедеятельности. С другой — динамика КЖК
свидетельствует об улучшении энергообеспечения колоноцитов и стимуляции
моторики кишечника, что подтверждается клиническими данными.
Изменение профиля кислот, динамика
значений АИ и уровня изокислот после лечения свидетельствуют о восстановлении
качественного состава микроорганизмов, баланса аэробных/анаэробных популяций
микроорганизмов, восстановлении внутрипросветной среды обитания
микроорганизмов, нормализации процессов протеолиза.
Полученные результаты позволили сделать
вывод о высокой эффективности Нормофлорина Л и Б в лечении ФЗК с синдромом
запора [29].
Наряду с гастроэнтерологами, биокомплексы
Нормофлорин Л, Б, Д используются в клинической практике врачами других
профилей, например эндокринологами, дерматологами, гинекологами.
Например, Нормофлорин Л и Б успешно включается
в терапевтические схемы больных метаболическим синдромом и ожирением.
Отмечаются положительные сдвиги в липидном обмене, снижении уровня холестерина,
некотором снижении гипогликемии, а также снижении кровяного давления [32].
Часто развитие кожных заболеваний
связывают с патологией ЖКТ, т. к. такие изменения в кишечнике, как
нарушение всасывания пищи, развитие и прогрессирование интоксикации, нарушение
кислотно-щелочного равновесия, могут отражаться в т. ч. и на коже.
Поврежденный эпидермис – это место колонизации различных, в т. ч. и
патогенных, бактерий. Благодаря тому, что биокомплексы Нормофлорин хорошо
переносятся больными и обладают пролонгированным действием, они тем самым
способствуют биокоррекции пиодермии, фолликулитов, сикозов, заедов,
гидраденита, кандидоза, острых баланопоститов, угревой сыпи [33].
В отзывах о клиническом применении
биокомплексов Нормофлорин Л и Б сообщается, что у больных после выполненных
нейрохирургических вмешательств по поводу тяжелой черепно-мозговой травмы,
нейроонкологической патологии, повреждений позвоночника, дискогенных
радикулитов отмечался хороший терапевтический эффект при комплексной терапии,
связанный, в частности, с устранением раздражения кожных покровов и предотвращением
пролежней. Кроме того, терапевтический эффект был более выраженным при
применении Нормофлорина в сравнении с лиофилизированными формами
бифидобактерий, назначенными для тех же целей больным контрольной группы [34].
В одном из недавних исследований изучалась
эффективность применения пробиотиков Нормофлорин Д в профилактике
антибиотик-ассоциированной диареи у больных на фоне приема системной
антибактериальной терапии в рамках комплексного лечения
оториноларингологической патологии [35].
Было проведено открытое рандомизированное
сравнительное исследование в параллельных группах. В исследовании приняли
участие 120 пациентов с оториноларингологической патологией в возрасте от 17
лет. Пациенты были рандомизированы в две группы в соотношении 1:1. Всем
пациентам была назначена стандартная системная антибиотикотерапия длительностью
не менее 5 и не более 14 дней и необходимые сопутствующие препараты согласно
утвержденным Минздравом РФ клиническим рекомендациям «Острый синусит», «Острый
средний отит», «Гипертрофия аденоидов», «Острый тонзиллофарингит». Кроме того,
первая группа (n = 60) принимала пробиотик группы нормофлоринов: 30 мл (3 ст.
л.) внутрь за 30 мин до еды (спустя 2–4 ч от приема антибиотика) 2 р/сут не
менее 14 дней. Вторая группа (n = 60) пробиотик группы нормофлоринов не
получала. Полученные результаты продемонстрированы на рис. 2 [35].
Рисунок 2. Частота
развития антибиотик-ассоциированной диареи в течение 30-дневного наблюдения за
пациентами обеих групп с момента назначения антибиотика системного действия
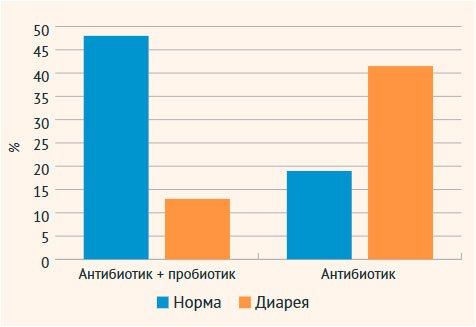
Из рис.
2 видно, что в основной группе только у 13 (21,7%) человек отмечалась ААД,
в то время как у остальных 47 (78,3%) пациентов расстройства стула не было.
Данные в группе контроля были противоположными: только у 19 (31,7%) человек не
было расстройства стула, в то время как у 41 (68,3%) пациента была ААД.
Авторами исследования на примере комплекса
Нормофлорин Д было продемонстрировано, что пробиотики позволяют в 78,3% случаев
предупредить и исключить развитие ААД у пациентов, получающих системную
антибактериальную терапию в рамках комплексного лечения
оториноларингологической патологии, что, безусловно, положительно сказывается
на качестве жизни пациентов. В связи с этим авторы сделали вывод о значимости и
целесообразности дополнения системной антибактериальной терапии пробиотиками, а
именно биологически активными добавками, являющимися источниками бифидо- и
лактобактерий, для восстановления микробиоценоза кишечника, нарушенного на фоне
приема антибиотиков [35].
Одним из актуальных и дискутируемых в
научной среде в настоящее время является вопрос о необходимости применения
пробиотиков у беременных женщин и новорожденных детей, особенно у младенцев,
родившихся в критическом состоянии. Несмотря на доказанную эффективность
пробиотиков в составе комплексной терапии антибиотик-ассоциированной и
нозокомиальной диареи, некротизирующего энтероколита, инфекции Helicobacter
pylori в некоторых клинических ситуациях, по-прежнему часто требуются
дальнейшие исследования, подтверждающие положительный эффект, определяющие тип,
дозу и время приема определенного пробиотического продукта.
С.Н. Денисова и соавт. в своем
исследовании оценивали влияние пробиотика L. reuteri protectis на
метаболическую активность кишечной микрофлоры беременных женщин и микробиом
новорожденных [36].
Под наблюдением находились 236 женщин в
возрасте от 21 до 42 лет в период беременности с 28-й до 42-й нед. гестации,
затем в течение 3 мес. после родов в качестве кормящих матерей. Беременные
женщины были распределены на две группы: основную, 140 пациенток которой в III
триместре в течение 3 нед. принимали пробиотик L. reuteri protectis, и
контрольную, 96 человек, где указанный препарат не назначался.
Для определения функционального состояния
кишечного микробиома у беременных женщин проводилась оценка эндогенных
биомаркеров его метаболической активности КЖК в копрофильтратах. Для разделения
и количественного определения КЖК в фекалиях использовался метод газовой
хроматографии – масс-спектрометрии. Оценка показателей КЖК проводилась в обеих
группа с интервалом в три недели.
Анализ показателей уровней КЖК у
беременных основной группы до приема пробиотика и в группе сравнения показал
низкие концентрации уксусной и пропионовой кислот, а также общего содержания
КЖК в копрофильтратах у беременных обеих групп, что свидетельствовало о
снижении метаболической активности молочнокислой флоры. Через 3 нед. от начала
приема L. reuteri protectis у беременных основной группы отмечалось
статистически значимое увеличение концентрации уксусной (p < 0,01) и
пропионовой кислот (p < 0,05), общего уровня КЖК (p < 0,05) с тенденцией
к повышению показателей масляной кислоты в копрофильтратах. В группе сравнения
через 3 нед. значимых изменений указанных показателей не отмечалось.
Поскольку наиболее частой соматической
патологией у беременных были аллергия и патология со стороны ЖКТ, то
дополнительно оценивалась динамика значений КЖК у женщин с указанными соматическими
заболеваниями до и после приема пробиотика. Оказалось, что после приема L.
reuteri protectis у беременных с указанными заболеваниями показатели КЖК в
копрофильтратах были выше, чем в группе сравнения. Наиболее низкие показатели
уксусной, пропионовой кислоты, общего уровня КЖК отмечались у женщин в группе
сравнения, не принимавшей пробиотических средств.
Авторы работы обратили внимание на низкую
концентрацию изокислот в копрофильтратах у всех наблюдаемых беременных, что
указывало на низкую активность протеолитических бактерий. Однако на фоне приема
L. reuteri protectis уровень изокислот в основной группе беременных
повышался в 1,5 раза.
Общий уровень метаболитов в кале был также
ниже физиологической нормы в обеих группах, что указывало на снижение метаболической
активности микрофлоры кишечника, недостаточное ее количественное и качественное
разнообразие вследствие функциональной недостаточности и однообразия пищевых
субстратов. Уровень анаэробного индекса в кале был подвержен отрицательному
смещению у всех женщин независимо от приема пробиотика, отражая преобладание
процессов брожения в кишечнике, нарушение инфраструктуры кишечного
микробиоценоза, снижение анаэробиоза среды, угнетение популяции анаэробной
микрофлоры.
Полученные результаты свидетельствуют о
повышении на фоне применения пробиотика функциональной активности кишечной
микробиоты, улучшении утилизации данных кислот колоноцитами, изменении состава
анаэробно-аэробных популяций микроорганизмов, приводящих к улучшению
окислительно-восстановительного потенциала кишечной среды. Авторы подтвердили
целесообразность приема пробиотиков, в частности Нормофлорина, в период
беременности в целях положительного влияния на состав провоспалительного
микробиома кишечника, активации иммунологического и метаболического созревания,
профилактики развития антибиотикорезистентности и кишечного резистома у плода и
новорожденного [36].
Таким образом, представленный обзор
свидетельствует о повышенном интересе научного медицинского сообщества не
только к роли нарушений баланса кишечной микробиоты в возникновении,
формировании клинических проявлений и прогрессировании различных заболеваний,
но и к поиску наиболее рациональных схем их коррекции [37–39].
Заключение
Начиная с 1990-х гг. создание синбиотиков
(syn – совместный, bios – жизнь), представляющих собой рациональные комбинации
консорциумов микроорганизмов нормальной кишечной микробиоты и функциональных
добавок, оказывающих пребиотические эффекты, стало одной из перспективных стратегий
в области применения средств для улучшения состояния кишечной микробиоты.
Пробиотики и пребиотики в составе синбиотиков действуют синергически,
обеспечивая комбинированную пользу: пребиотики способствуют выживанию и
активности проверенных пробиотиков in vivo, а также оказывают стимулирующее
воздействие на рост и метаболизм местной анаэробной микробиоты. Механизмы
влияния синбиотиков на организм человека тщательно изучаются. При этом
терапевтический эффект синбиотика в значительной мере зависит от индивидуальной
комбинации про- и пребиотика. С одной стороны, это влечет за собой определенную
ограниченность их применения, с другой, учитывая огромное количество возможных
комбинаций, открывает многообещающие перспективы.
Биокомплексы Нормофлорин представляют собой
эффективные препараты для лечения пациентов, страдающих антибиотик-ассоциированной
диареей, функциональными заболеваниями кишечника с синдромом запора, СРК,
язвенной болезнью, метаболическими нарушениями, заболеваниями лор-органов,
дерматологическими и гинекологическими заболеваниями.
При терапии Нормофлорином наблюдается:
- нормализация двигательной активности
кишечника; - происходят положительные сдвиги в
составе экосистемы толстой кишки, заключающиеся в изменении метаболической
активности толстокишечной микрофлоры и ее родового состава, нормализации
анаэробно-аэробных взаимоотношений, восстановлении внутриполостного окислительно-восстановительного
потенциала внутрипросветной среды; - устраняются явления кишечной диспепсии
(урчание, метеоризм).
Биокомплексы Нормофлорин характеризуются
хорошей переносимостью и безопасностью. Положительный эффект приема данных
продуктов сохраняется минимум в течение двух недель.
Все вышеизложенное позволяет рекомендовать
биокомплексы Нормофлорин в комплексе лечения различных заболеваний.
[1] WGO Global Guidelines and Cascades
2017. Probiotics and Prebiotics. Available at: http://worldgastroenterology.org; World
Gastroenterology Organisation Global Guidelines Probiotics and Prebiotics.
February 2023: Available at: http://worldgastroenterology.org.
Список литературы / References
Развернуть
- Ардатская МД. Микробиоценоз кишечника и его роль в развитии и поддержании заболеваний желудочно-кишечного тракта. Новости медицины и фармации. 2010;(313):68.. Режим доступа: http://www.mif-ua.com/archive/article/11927.
- Ардатская МД. Роль низкомолекулярных метаболитов кишечной микробиоты в патогенезе, диагностике и профилактике колоректального рака. Экспериментальная и клиническая гастроэнтерология. 2017;(3):13-21. Режим доступа: https://www.nogr.org/jour/article/view/661.
- Ардатская МД, Гарушьян ГВ, Мойсак РП, Топчий ТБ. Роль короткоцепочечных жирных кислот в оценке состояния микробиоценоза кишечника и его коррекции у пациентов с НАЖБП различных стадий. Экспериментальная и клиническая гастроэнтерология. 2019;161(1):106-116. https://doi.org/10.31146/1682-8658-ecg-161-1-106-116.
- Чиркин ВИ, Ардатская МД, Лазарев ИА. Долгосрочные эффекты препарата пищевых волокон псиллиума (Мукофальк) у пациентов с метаболическим синдромом. Клинические перспективы гастроэнтерологии, гепатологии. 2012;(1):34-42. Режим доступа: https://www.mucofalk.ru/publications/dolgosrochnye-effekty-preparata-pishhevyh-volokon-psilliuma-mukofalk-upaczientov-s-metabolicheskim-sindromom.
- Ардатская МД, Топчий ТБ, Буторова ЛИ, Туаева ЕМ, Саютина ЕВ. Антибиотико-ассоциированные поражения кишечника в практике клинициста. М.: Прима Принт; 2020. 53 с.
- Ардатская МД, Масловский ЛВ, Зверков ИВ. Коррекция нарушений микробиоты кишечника при хроническом панкреатите. Экспериментальная и клиническая гастроэнтерология. 2021;195(11):52-59. https://doi.org/10.31146/1682-8658-ecg-195-11-52-59.
- Шендеров БА, Степанчук ЮБ, Манвелова МА. Пробиотики и функциональное питание. Антибиотики и химиотерапия. 1997;42;(7):30-34. Режим доступа: http://elib.fesmu.ru/Article.aspx?id=11474.
- Gogineni VK, Morrow LE, Gregory PJ, Malesker MA. Probiotics: History and Evolution. J Anc Dis Prev Rem. 2013;1:107. https://doi.org/10.4172/2329-8731.1000107.
- Patel1 R, DuPont HL. New Approaches for Bacteriotherapy: Prebiotics, New-Generation Probiotics, and Synbiotics. CID. 2015;60(Suppl. 2):108-121. https://doi.org/10.1093/cid/civ177.
- Ivashkin V, Drapkina O, Poluektova Ye, Kuchumova S, Sheptulin A, Shifrin O. The effect of a multi-strain probiotic on the symptoms and small intestinal bacterial overgrowth in constipation-predominant irritable bowel syndrome: A randomized, simpleblind, placebo-controlled trial. Am J Clin Med Res. 2015;3(2):18-23. https://doi.org/10.12691/ajcmr-3-2-1.
- Forssten SD, Ouwehand AC. Simulating colonic survival of probiotics in singlestrain products compared to multi-strain products. Microb Ecol Health Dis. 2017;28(1):1378061. https://doi.org/10.1080/16512235.2017.1378061.
- Ардатская МД. Пробиотики, пребиотики и метабиотики в клинической практике. М.: ГЭОТАР-Медиа; 2024. 264 с.
- Андреева ИВ, Стецюк ОУ. Место пробиотиков в практических рекомендациях по гастроэнтерологии: реальность и ближайшие перспективы. Consilium Medicum. 2018;20(8):67-72. https://doi.org/10.26442/2075-1753_2018.8.67-72.
- Sanders ME, Merenstein DJ, Reid G, Glenn R Gibson, Robert A Rastall. Probiotics and prebiotics in intestinal health and disease: from biology to the clinic. Nat Rev Gastroenterol Hepatol. 2019;10:605-616. https://doi.org/10.1038/s41575-019-0173-3.
- Плотникова ЕЮ, Захарова ЮВ. Иммуномодулирующие эффекты пробиотиков. Медицинский совет. 2020;(15):135-144. https://doi.org/10.21518/2079-701X-2020-15-135-144.
- Deshpande G, Rao S, Patole S, Bulsara M. Updated meta-analysis of probiotics for preventing necrotizing enterocolitis in preterm neonates. Pediatrics. 2010;125(5):921-930. https://doi.org/10.1542/peds.2009-1301.
- McFarland LV, Huang Y, Wang L, Malfertheiner P. Systematic review and metaanalysis: Multi-strain probiotics as adjunct therapy for Helicobacter pylori eradication and prevention of adverse events. United European Gastroenterol J. 2016;4(4):546-561. https://doi.org/10.1177/2050640615617358.
- Das TK, Pradhan Sh, Chakrabarti S, Mondal K, Ghosh Kl. Current Status of Probiotic and related Health Benefits. Appl Food Res. 2022;2:100185. https://doi.org/10.1016/j.afres.2022.100185.
- Shin A, Preidis GA, Shulman R, Kashyap PC. The Gut Microbiome in Adult and Pediatric Functional Gastrointestinal Disorders. Clin Gastroenterol Hepatol. 2019;17:256-274. https://doi.org/10.1016/j.cgh.2018.08.054.
- He Y, Zhu L, Chen J, Tang X, Pan M, Yuan W, Wang H. Efficacy of Probiotic Compounds in Relieving Constipation and Their Colonization in Gut Microbiota. Molecules. 2022;27(3):666. https://doi.org/10.3390/molecules27030666.
- Shafiei M, Mardi S, Ghadimi S, Poorshahbazi H, Pourabbas R, Keykhah M, Rafiemanesh H. Efficacy and tolerability of probiotics, prebiotics, and symbiotics consumption on oral complications of patients with thyroid and head and neck cancers: a systematic review and meta-analysis. BMC Oral Health. 2025;25(1):677. https://doi.org/10.1186/s12903-025-05876-9.
- De la Rosa González A, Guerra-Ojeda S, Camacho-Villa MA, Valls A, Alegre E, Quintero-Bernal R et al. Effect of Probiotics on Gastrointestinal Health Through the Aryl Hydrocarbon Receptor Pathway: A Systematic Review. Foods. 2024;13(21):3479. https://doi.org/10.3390/foods13213479.
- Zhao S, Lu Z, Zhao F, Tang S, Zhang L, Feng C. Assessing the impact of probiotics on immunotherapy effectiveness and antibiotic-mediated resistance in cancer: a systematic review and meta-analysis. Front Immunol. 2025;16:1538969. https://doi.org/10.3389/fimmu.2025.1538969.
- Минушкин ОН, Бондаренко ВМ, Шапошникова ЛИ. Эффективность «Нормофлорина-Д» при антибактериальной терапии. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. Тверь: Триада; 2009. С. 28-33.
- Молина ЛП, Гусакова ЕВ, Эфендиева МТ. Изучение эффективности биокомплексов «Нормофлорин Л» и «Нормофлорин Б» в терапии синдрома раздраженного кишечника. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. Тверь: Триада; 2009. C. 26-28.
- Еремина ЕЮ. Воспалительный процесс тонкой кишки как отражение побочного эффекта эрадикационной терапии язвенной болезни и его коррекция с помощью синбиотических препаратов. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. Тверь: Триада; 2009. C. 34-47.
- Лоранская ИД, Батюхно ТА. Иммуномодулирующий эффект Биокомплекса Нормофлорин Д у больных хроническим панкреатитом. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. М.: Триада; 2009. С. 61-65.
- Ткаченко ЕИ. Оптимизация лечения синбиотиками больных с целиакией. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. Тверь: Триада; 2009. C. 68-72. Режим доступа: http://www.ncderm.ru/i/info.php?id=21824.
- Ардатская МД, Минушкин ОН. Пробиотики в лечении функциональных заболеваний кишечника. Экспериментальная и клиническая гастроэнтерология. 2012;(3):106-113. Режим доступа: https://www.elibrary.ru/rwhgyx.
- Кондратьева ЕН (ред.). Метаболизм бактерий. М.: Мир; 1982. 310 с.
- Macfarlane GT, Macfarlane S. Human colonic microbiota: ecology, physiology and metabolic potential of intestinal bacteria. Scand J Gastroenterol. 1997;32(Sup222):3-9. https://doi.org/10.1080/00365521.1997.11720708.
- Турова ЕА, Бондаренко ВМ, Шапошникова ЛИ. Биокомплексы «Нормофлорин Л» и «Нормофлорин Б» в комплексном лечении больных метаболическим синдромом и ожирением. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. Тверь: Триада; 2009. С. 74-78.
- Герасимчук ЕВ. Применение жидких синбиотиков «Нормофлорин Л» и «Нормофлорин-Б» в комплексном лечении кожно-венерологических пациентов в условиях поликлиники. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. Тверь: Триада; 2009. C. 78-81.
- Амчеславский ВГ, Бондаренко ВМ, Шапошникова ЛИ. Отзыв по клиническому применению биокомплексов «Нормофлорин Л» и «Нормофлорин Б» у нейрохирургических больных. В: Бондаренко ВМ, Шапошникова ЛИ (ред.). Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. Тверь: Триада; 2009. С. 90-91.
- Баранов КК, Акопян АН. Профилактика развития антибиотик-ассоциированной диареи у пациентов, получавших системную антибактериальную терапию по поводу оториноларингологических заболеваний. Детская оториноларингология. 2024;(1-2):34-37. Режим доступа: https://cdn.lifehacker.ru/wp-content/uploads/2025/05/Baranov-Akopyan_Medici_KidLOR_1_2024_1748002041.pdf.
- Денисова СН, Сахарова ЕС, Ильенко ЛИ, Богданова СВ, Тарасова ОВ, Ильяшенко ВА и др. Влияние пробиотиков на функциональную активность кишечной микробиоты беременных и микробиом новорожденных. Вопросы практической педиатрии. 2024;19(2):23-32. https://doi.org/10.20953/1817-7646-2024-2-23-32.
- Markowiak P, Slizewska K. Effects of Probiotics, Prebiotics, and Synbiotics on Human Health. Nutrients. 2017;9:1021. https://doi.org/10.3390/nu9091021.
- Раскина КВ, Мартынова ЕЮ, Фатхутдинов ИР, Потешкин ЮЕ. Современные бактериологические препараты: влияние на микробиоту кишечника и роль в лечении заболеваний. РМЖ. 2018;(5-2):86-91.. Режим доступа: https://www.rmj.ru/articles/pediatriya/Sovremennye_bakteriologicheskie_preparaty_vliyanie_namikrobiotu_kishechnika_iroly_vlechenii_zabolevaniy
- Харитонова ЛА, Григорьев КИ, Борзакова СН. Микробиота человека: как новая научная парадигма меняет медицинскую практику. Экспериментальная и клиническая гастроэнтерология. 2019;161(1):55-63. https://doi.org/10.31146/1682-8658-ecg-161-1-55-63.
Фото:
Fantastic Studio//FOTODOM/Shutterstoсk



 1
1 2
2 3
3 4
4


Комментарии (0)