
Журнал "Медицинский совет" №4/2024
DOI: 10.21518/ms2024-114
О.И. Лисицына, ORCID: 0000-0002-7775-3508
Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова; 117997, Россия, Москва, ул. Академика Опарина, д. 4
Гестационный сахарный диабет (ГСД) является одним из самых распространенных заболеваний во время беременности и повышает риск краткосрочных и долгосрочных осложнений как для матери, так и для потомства. Своевременно проведенная терапия ГСД достоверно снижает указанные риски. Развитие инсулинорезистентности во время беременности связано с увеличением со сроком беременности материнских и фетоплацентарных гормонов (плацентарный лактоген, эстрогены и прогестерон, кортизол и пролактин). Таким образом, ГСД формируется во время беременности у пациентов с недостаточной функцией поджелудочной железы на фоне прогрессирующей гипергликемии и инсулинорезистентности. Для установки диагноза в мировой практике принято проведение перорального глюкозотолерантного теста (ПГТТ). ПГТТ в России выполняется в сроке 24–28 нед. беременности с использованием 75 г глюкозы и оценкой гликемии венозной плазмы в трех точках: до приема раствора глюкозы и через 60 и 120 мин после приема. Однако одной из проблем, связанных с ПГТТ, является отказ пациенток от его прохождения. Самой часто называемой причиной несогласия проведения ПГТТ являются тошнота и рвота. В ряде случаев пациенты не могут выполнить тест по причине тяжелой переносимости гиперосмолярного раствора глюкозы. Для подобных случаев в литературе обсуждаются ряд решений, одним из которых называется возможное применение композиций на основе глюкозы с разрешенными во время беременности вкусовыми добавками, улучшающими переносимость ПГТТ. Улучшение переносимости и комплаентности процедуры – одно из важнейших условий успешной и своевременной диагностики.
Для цитирования: Лисицына ОИ. Пероральный глюкозотолерантный тест во время беременности: вопросы и ответы. Медицинский совет. 2024;18(4):98–102. https://doi.org/10.21518/ms2024-114.
Конфликт интересов: автор заявляет об отсутствии конфликта интересов.
Обмен исследовательскими данными: данные, подтверждающие выводы исследования, доступны по запросу у автора, ответственного за переписку, после одобрения ведущим исследователем.
Oral glucose tolerance test in pregnancy: questions and answers
Olga I. Lisitsyna, ORCID: 0000-0002-7775-3508
Kulakov National Medical Research Center of Obstetrics, Gynecology and Perinatology; 4, Academician Oparin St., Moscow, 117997, Russia
Gestational diabetes mellitus (GDM) is one of the most common diseases during pregnancy and increases risks of short- and long-term complications to both mothers and their children. Timely treatment of GDM significantly reduces the specified risks. The development of insulin resistance in pregnancy is associated with increased secretion of maternal and fetoplacental hormones (placental lactogen, estrogens and progesterone, cortisol and prolactin) with increasing gestational age. Thus, GDM develops during pregnancy in patients with insufficient pancreatic function due to progressive hyperglycemia and insulin resistance. Oral glucose tolerance test (OGTT) is the most commonly used test in world practice to establish a diagnosis. In Russia, OGTT is carried out at a gestational age of 24–28 weeks using 75 g of glucose and assessing venous plasma glycemia values at three points: before and 30, 60, and 120 minutes after drinking the glucose solution. However, refusal of patients to complete the test is one of the problems associated with the OGTT. Nausea and vomiting are the most commonly reason for not completing the OGTT. In some cases, patients cannot complete the test due to severe tolerance to a hyperosmolar glucose solution. In such cases, a number of solutions are discussed in the literature, one of which is the possible use of glucose-based compositions comprising flavouring additives, which are allowed for use during pregnancy to improve the tolerability of the OGTT. Improving the tolerability and compliance with the procedure is one of the most important conditions for successful and timely diagnosis.
For citation: Lisitsyna OI. Oral glucose tolerance test during pregnancy: questions and answers. Meditsinskiy Sovet. 2024;18(4):98–102. (In Russ.) https://doi.org/10.21518/ms2024-114.
Conflict of interest: the author declare no conflict of interest.
Research data sharing: derived data supporting the findings of this study are available from the corresponding author on request after the Principal Investigator approval.
Введение
Сахарный диабет 2-го типа (СД2) относят к самым распространенным экономически значимым хроническим заболеваниям во всем мире, численность болеющих которым достигает 100 млн человек. Учитывая значительное патогенетическое сходство (недостаточная секреция инсулина в условиях возрастающей инсулинорезистентности), одним из факторов риска развития СД2 выступает гестационный сахарный диабет (ГСД), распространенность которого среди беременных достигает 16% в разных странах [1–3]. Развитие инсулинорезистентности во время беременности связано с увеличением со сроком беременности материнских и фетоплацентарных гормонов (плацентарный лактоген, эстрогены и прогестерон, кортизол и пролактин). Таким образом, ГСД формируется во время беременности у пациентов с недостаточной функцией поджелудочной железы на фоне прогрессирующей гипергликемии и инсулинорезистентности [4]. В большинстве случаев ГСД не имеет ярких клинических появлений, характерных для СД, однако ассоциирован с повышением ряда краткосрочных и долгосрочных рисков как для матери, так и для потомства (табл. 1) [5–7]. При этом своевременно проведенная терапия достоверно снижает краткосрочные риски. Поэтому высокую актуальность имеет эффективная диагностика и терапия ГСД у беременных.
Таблица 1. Краткосрочные и долгосрочные риски гестационного сахарного диабета
| • Гипертензивные осложнения беременности • Макросомия плода (дистоция плечиков, родовая травма) • Оперативное родоразрешение • Перинатальная смертность • Неонатальные метаболические осложнения (гипогликемия, гипербилирубинемия, гипокальциемия) | • Развитие СД2 • Развитие метаболического синдрома • Развитие сердечно-сосудистых заболеваний | • Ожирение • Метаболический синдром • Нарушение толерантности к глюкозе • Гипертензивные нарушения |
ГСД – заболевание, характеризующееся гипергликемией, впервые выявленной во время беременности, но не соответствующей критериям «манифестного» сахарного диабета [8]. Для диагностики ГСД в нашей стране применяется следующая стратегия: первым этапом на ранних сроках беременности или при первом посещении врача всем беременным назначается исследование глюкозы венозной плазмы натощак, при отсутствии выявленных нарушений углеводного обмена проводится пероральный глюкозотолерантный тест (ПГТТ) с 75 г глюкозы на сроке 24–28 нед. гестации (табл. 2) [1].
Таблица 2. Критерии диагностики гестационного сахарного диабета по результатам перорального глюкозотолерантного теста
| Натощак | ≥5,1, но <7,0 |
| Через 1 ч | ≥10,0 |
| Через 2 ч | ≥8,5, но <11,1 |
Так, критерием постановки ГСД на любом сроке беременности является выявление глюкозы в венозной плазме натощак ≥ 5,1 ммоль/л. При выявлении гликемии натощак ≥ 7,0 ммоль/л проводится дополнительное обследование для подтверждения или исключения манифестного СД [1].
Какие существуют варианты перорального глюкозотолерантного теста? Отечественный и зарубежный опыт
В мире существует два подхода для проведения ПГТТ: одноступенчатый и двухступенчатый. Одноступенчатый подход принят и применяется в России и представляет из себя глюкозотолерантный тест с 75 г глюкозы (рекомендован ВОЗ и Международной ассоциацией групп изучения диабета и беременности, англ. International Association of Diabetes and Pregnancy Study Groups, IADPSG).
Двухступенчатый тест (рекомендован Американской коллегией акушеров и гинекологов, англ. American College of Obstetricians and Gynecologists – ACOG; предлагается Американской ассоциацией сахарного диабета, англ. American Diabetes Association – ADA) проводится также в сроке 24–28 нед. беременности, но включает два этапа. Первым этапом проводят скрининг-тест с 50 г глюкозы и исследованием уровня гликемии через 60 мин. Указанная часть может выполняться независимо от приема пищи или времени суток. Пациенткам с повышенными значениями выполняют второй этап – трехчасовой тест со 100 г глюкозы [1, 9].
Считается, что указанные подходы обладают сопоставимой диагностической ценностью. С одной стороны, относительное удобство двухступенчатого подхода состоит в легкости проведения скринингового теста с 50 г глюкозы, что позволяет охватить большее количество пациенток на первом этапе, с другой стороны, тест со 100 г глюкозы обладает худшей переносимостью в сравнении с 75 г глюкозы [9].
Когда и как проводится пероральный глюкозотолерантный тест? Какая нужна подготовка перед глюкозотолерантным тестом?
Учитывая рекомендации ВОЗ, а также результаты исследования HAPO, оптимальный рекомендованный срок для выполнения ПГТТ – это 24–28 нед. беременности [10, 11]. В случае выявления факторов высокого риска ГСД исследование может выполняться до 32 нед., но не позднее [1, 5]. Тест проводят в несколько шагов, оценка гликемии венозной плазмы оценивается в трех точках: 1-я точка – натощак, 2-я и 3-я точки – через 60 и 120 мин после приема раствора с 75 г глюкозы (глюкозу растворяют в 250–300 мл теплой негазированной воды) соответственно. В ходе выполнения теста пациентке необходимо сидеть, возможен прием дополнительной воды, курение не допускается. Прием лекарственных средств пациенткой по возможности осуществляется после завершения исследования. ПГТТ выполняют после 8-часового ночного голодания, последний прием пищи должен обязательно содержать 30–50 г углеводов, что соответствует 3 кускам хлеба или 6 ложкам каши [12]. Интерпретация результатов тестирования может быть проведена акушером-гинекологом, терапевтом, семейным врачом или эндокринологом. Ведение пациентов с ГСД осуществляется в большей степени акушерами-гинекологами, при неэффективности диетотерапии назначается консультация эндокринолога.
Какие могут возникнуть проблемы с проведением перорального глюкозотолерантного теста?
В ряде случаев проведение ПГТТ может быть противопоказано: диагностированный СД, индивидуальная непереносимость глюкозы, демпинг-синдром, обострение заболеваний желудочно-кишечного тракта, тошнота и рвота, необходимость соблюдения постельного режима [1, 8, 12]. В указанных обстоятельствах рекомендовано проводить оценку гликемии натощак.
Другой проблемой, связанной с ПГТТ, является отказ пациенток от его выполнения. Так, согласно исследованиям, до 40% беременных не соблюдают рекомендации по ПГТТ и пропускают его [13–15]. Следует подчеркнуть, что большинство пациенток, отказавшихся от ПГТТ, считают, что указанное исследование может нанести какой-либо вред им самим или их ребенку. Другая часть считают, что выполнение ПГТТ необязательно, ссылаясь на неосложненное течение предыдущей беременности. Кроме того, некоторые пациентки отмечают, что не выполнили ПГТТ, т. к. их доктор им этого не рекомендовал или они слышали негативную информацию о ПГТТ из источников массмедиа [16]. Среди иных причин отказа от тестирования пациентки указывали плохую транспортную доступность медицинских центров, сложность в посещении множества визитов к врачу [15].
Так, согласно исследованию, выполненному в Британии и включавшему 1 906 беременных женщин, реже комплаентны для выполнения ПГТТ пациентки более молодого возраста, низкого социально-экономического статуса, представители малых этнических групп, а также с высоким паритетом [15].
Самой распространенной причиной отказа от ПГТТ является тошнота и рвота [13–17]. Часть пациентов не может выполнить тест по причине тяжелой переносимости гиперосмолярного раствора глюкозы. Подобный высококонцентрированный раствор может вызывать раздражение желудка, задержку его опорожнения и, как следствие, тошноту и рвоту [17].
Для подобных ситуаций в литературе обсуждаются следующие решения:
- В случае если у пациентки во время ПГТТ произошла рвота, тестирование может быть повторно выполнено в другой день с возможным предварительным приемом антиэметиков (противорвотных средств).
- Охлаждение приготовленного раствора с помощью льда также может снизить чувство тошноты и рвоту.
- В исключительных случаях описывается применение определенных продуктов (коммерческие конфеты, снеки и т. д.), содержащих эквивалентное количество глюкозы [18, 19].
- Кроме того, в литературе встречаются упоминания о возможном внутривенном введении глюкозы [20].
В случаях когда описанные методы не оказывают эффекта или не могут быть выполнены, возможно проведение оценки гликемии самостоятельно пациенткой с ведением дневника [21].
Улучшение переносимости перорального глюкозотолерантного теста. Возможное решение
В настоящее время в России возможно применение композиций на основе глюкозы (D-глюкозы, декстрозы), которые могут содержать разрешенные во время беременности вкусовые добавки, не влияя при этом на результаты ПГТТ [22]. Так, например, добавление лимонного ароматизатора положительно влияет на вкусовые качества раствора и, таким образом, улучшает переносимость теста, уменьшает тошноту.
Одним из указанных лекарственных средств, представленных на отечественном рынке, является препарат Глюкоза, ЛП-№(003192)-(РГ-RU), в форме порошка для приготовления раствора для приема внутрь с несколькими вариантами вкусов (действующее вещество 75 г безводной декстрозы). Препарат зарегистрирован ООО ГТТ и производится компанией ООО «ФармМентал групп». Особенностью указанного лекарственного средства является его запатентованный состав с безопасными (разрешенными во время беременности, не обладающими тератогенным или эмбриотоксическим действием) добавками: лимонной и адипиновой кислотой, обладающими синергетическим действием в снижении тошноты и рвоты, в сравнении со стандартными препаратами чистой глюкозы (декстрозы) и композициями, содержащими только один из указанных компонентов. Кроме того, по наблюдениям авторов и данным патента, добавление вкусовых добавок (клубничной, апельсиновой, ананасовой) в указанный состав положительно воспринималось пациентами, отмечающими приятный вкус [22].
Дополнительное исследование-анкетирование выполнено производителем указанного лекарственного средства ООО «ФармМентал групп». Проведено анкетирование 71 беременной женщины (средний возраст составил 29 лет): 37 участников, прошедших ПГТТ с использованием препарата Глюкоза (52%), и 34 участника – стандартного раствора глюкозы (48%).
После проведения ПГТТ участникам предлагалось пройти анкетирование с оценкой своего состояния (общее самочувствие, головная боль, тошнота, головокружение, боли в животе, слабость и повышенное потоотделение) в баллах – от 0 баллов (нет симптомов) до 4 баллов по каждому показателю, сумма баллов от минимального – 0 баллов до максимального – 36 баллов: чем выше балл, тем хуже состояние.
Дополнительный статистический анализ полученных данных проводился в программе Jamovi. Непрерывные переменные были представлены в виде среднего, медианы и межквартильных значений (Ме(Q1–Q3)). С целью определения статистической значимости различий непараметрических данных был выбран критерий Манна – Уитни. Для описания категориальных бинарных данных использовали абсолютные значения и процентные доли от общего числа в группе. Анализ качественных признаков проводили с помощью хи-квадрата Пирсона. Величину порогового уровня значимости p принимали равной 0,05. После ПГТТ средний балл в группе стандартного раствора составил 2,47 (признаки нарушения самочувствия отмечались у 18% опрошенных), в группе исследуемого препарата – 1,54 (признаки нарушения самочувствия отмечались у 11% участников). Медиана и межквартильные интервалы составили: для стандартного раствора – 2 (1– 4), для исследуемого препарата – 0 (0–2) (p = 0,023).
Признаки тошноты и слабости чаще отмечали участницы из группы стандартного раствора в сравнении с исследуемым препаратом (рис. 1). Чувство тошноты испытывали 11 участниц (30%) в группе исследуемого препарата в сравнении с 14 участницами (41%) в группе стандартного раствора (p = 0,313). На слабость указывали 10 участниц (27%) в группе исследуемого препарата в сравнении с 16 участницами (47%) в группе стандартного раствора (p = 0,08).
Рисунок 1. Балльная оценка самочувствия пациенток после перорального глюкозотолерантного теста
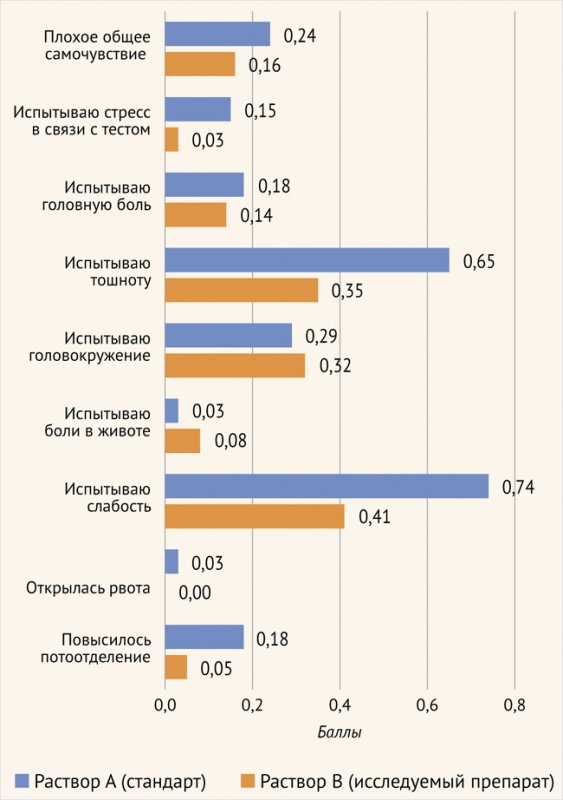
Дополнительно в анкетирование включены вопросы по оценке органолептических свойств растворов. Препарат Глюкоза был оценен респондентками как более удобный при приеме, с более приятным вкусом (54% пациенток из группы исследуемого препарата оценили на «отлично» в сравнении с 26% в группе стандартного раствора (p = 0,016)) и комфортным проглатыванием (51% пациенток из группы исследуемого препарата оценили на «отлично» в сравнении с 31% в группе стандартного раствора). Однако, данный показатель не достиг статистически значимой разницы (p = 0,06). Удовлетворенность цветом (p = 0,629) и запахом (p = 0,957) в исследуемых группах значительно не отличалась (рис. 2).
Рисунок 2. Оценка органолептических свойств исследуемых растворов
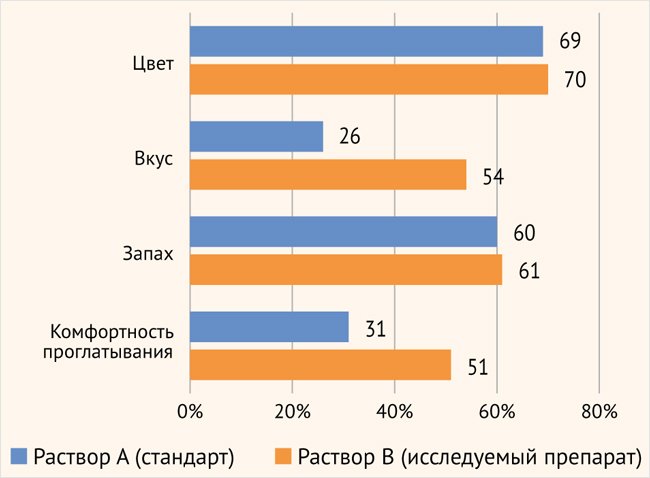
Кроме того, для пациенток, принимавших раствор Глюкоза и проходивших ПГТТ ранее в предыдущую беременность (n = 18), проведен опрос о переносимости исследования. Большинство участниц (83%) отметили лучшую переносимость ПГТТ с препаратом Глюкоза в сравнении со стандартным раствором.
Заключение
ГСД является одним из самых распространенных заболеваний во время беременности и повышает риск краткосрочных и долгосрочных осложнений как для матери, так и для потомства. Своевременно проведенная терапия ГСД достоверно снижает указанные риски. Для установки диагноза в мировой практике принято проведение ПГТТ. Однако одной их проблем, связанных с ПГТТ, является отказ пациенток от его прохождения. Самой часто называемой причиной несогласия проведения ПГТТ являются тошнота и рвота. Для подобных случаев в литературе обсуждаются ряд решений, одним из которых называется возможное применение композиций на основе глюкозы с разрешенными во время беременности вкусовыми добавками, улучшающими переносимость ПГТТ. Появление в арсенале врачей и лабораторий препарата Глюкоза с запатентованным составом для проведения ПГТТ может способствовать лучшему комплаенсу пациенток в отношении исследования.
Список литературы / References
Развернуть
- Шестакова ТП, Старостина ЕГ. Диагностика гестационного сахарного диабета. М.: Московский областной научно-исследовательский клинический институт им. М.Ф. Владимирского; 2023. 44 с.
- Белоцерковцева ЛД, Коваленко ЛВ, Каспарова АЭ, Васечко ТМ, Конченкова ЕН, Романова ВС. Эволюция диагностических критериев гестационного сахарного диабета. Вестник СурГУ. Медицина. 2014;21(3):9–16. Режим доступа: https://elibrary.ru/. / Belotserkovtseva LD, Kovalenko LV, Kasparova AE, Vasechko TM, Konchenkova EN, Romanova VS. The evolution of the diagnostic criteria of gestational diabetes. Vestnik SurGU. Medicina. 2014;21(3):9–16. (In Russ.) Available at: https://elibrary.ru/.
- Bilous RW, Jacklin PB, Maresh MJ, Sacks DA. Resolving the Gestational Diabetes Diagnosis Conundrum: The Need for a Randomized Controlled Trial of Treatment. Diabetes Care. 2021;44(4):858–864. doi: 10.2337/dc20-2941.
- Carr D, Gabbe S. Gestational Diabetes: Detection, Management and implications. Clinical Diabetes. 1988;16(1):4–11. Available at: https://web.archive.org/.
- HAPO Study Cooperative Research Group, Metzger BE, Lowe LP, Dyer AR, Trimble ER, Chaovarindr U, Coustan DR et al. Hyperglycemia and adverse pregnancy outcomes. N Engl J Med. 2008;358(19):1991–2002. doi: 10.1056/NEJMoa0707943.
- Ye W, Luo C, Huang J, Li C, Liu Z, Liu F. Gestational diabetes mellitus and adverse pregnancy outcomes: systematic review and meta-analysis. BMJ. 2022;377:e067946. doi: 10.1136/bmj-2021-067946.
- Venkatesh KK, Lynch CD, Powe CE, Costantine MM, Thung SF, Gabbe SG et al. Risk of Adverse Pregnancy Outcomes Among Pregnant Individuals With Gestational Diabetes by Race and Ethnicity in the United States, 2014–2020. JAMA. 2022;327(14):1356–1367. doi: 10.1001/jama.2022.3189.
- Дедов ИИ, Краснопольский ВИ, Сухих ГТ. Российский национальный консенсус гестационный сахарный диабет: диагностика, лечение, послеродовое наблюдение. Сахарный диабет. 2012;15(4):4–10. doi: 10.14341/2072-0351-5531. / Dedov II, Krasnopol’skiy VI, Sukhikh GT. Russian National Consensus Statement on gestational diabetes: diagnostics, treatment and postnatal care. Diabetes Mellitus. 2012;15(4):4–10. (In Russ.) doi: 10.14341/2072-0351-5531.
- ACOG Practice Bulletin No. 190: Gestational Diabetes Mellitus. Obstet Gynecol. 2018;131(2):e49–e64. doi: 10.1097/AOG.0000000000002501.
- Тажетдинов ЕХ, Костин ИН, Ли КИ, Аршинова ОВ, Чепорева ОН, Забирова СД, Пак ВЕ. Перспективы раннего скрининга гестационного сахарного диабета. Акушерство и гинекология. Новости. Мнения. Обучение. 2020;8(3):90–94. Режим доступа: https://cyberleninka.ru/. / Tazhetdinov EKh, Kostin IN, Li KI, Arshinova OV, Cheporeva ON, Zabirova SD, Pak VE. Prospects for early screening for gestational diabetes. Akusherstvo i Ginekologiya. Novosti, Mneniya, Obuchenie. 2020;8(3):90–94. (In Russ.) Available at: https://cyberleninka.ru/.
- Матейкович ЕА. Неблагоприятные исходы беременности и гестационный сахарный диабет: от исследования HAPO к современным данным. Акушерство и гинекология. 2021;(2):13–20. doi: 10.18565/aig.2021.2.13-20. / Mateikovich EA. Adverse pregnancy outcomes and gestational diabetes: from the HAPO study to current data. Akusherstvo i Ginekologiya (Russian Federation). 2021;(2): 13–20. (In Russ.) doi: 10.18565/aig.2021.2.13-20.
- Потешкин ЮЕ. Беременность. Пероральный глюкозотолерантный тест. Актуальная эндокринология. 2018;(2):81. Режим доступа: https://actendocrinology.ru/. / Poteshkin YuE. Pregnancy. Oral glucose tolerance test. Aktualnaya Ehndokrinologiya. 2018;(2):81. (In Russ.) Available at: https://actendocrinology.ru/.
- Hocaoglu M, Turgut A, Guzin K, Yardimci OD, Gunay T, Bor ED et al. Why some pregnant women refuse glucose challenge test? Turkish pregnant women’s perspectives for gestational diabetes mellitus screening. North Clin Istanb. 2018;6(1):7–12. doi: 10.14744/nci.2018.37167.
- Sezer H, Yazici D, Canbaz HB, Gonenli MG, Yerlikaya A, Ata B et al. The frequency of acceptance of oral glucose tolerance test in Turkish pregnant women: A single tertiary center results. North Clin Istanb. 2022;9(2):140–148. doi: 10.14744/nci.2021.80588.
- Lachmann EH, Fox RA, Dennison RA, Usher-Smith JA, Meek CL, Aiken CE. Barriers to completing oral glucose tolerance testing in women at risk of gestational diabetes. Diabet Med. 2020;37(9):1482–1489. doi: 10.1111/dme.14292.
- Aydogmus H, Aydogmus S, Tiras HI, Cankaya Z. Behaviors of Turkish pregnant women towards gestational diabetes screening. Pak J Med Sci. 2021;37(5):1486–1490. doi: 10.12669/pjms.37.5.4176.
- Fachnie JD, Whitehouse FW, McGrath Z. Vomiting during OGTT in third trimester of pregnancy. Diabetes Care. 1988;11(10):818. doi: 10.2337/diacare.11.10.818.
- Lamar ME, Kuehl TJ, Cooney AT, Gayle LJ, Holleman S, Allen SR. Jelly beans as an alternative to a fifty-gram glucose beverage for gestational diabetes screening. Am J Obstet Gynecol. 1999;181(5):1154–1157. doi: 10.1016/s0002-9378(99)70099-2.
- Racusin DA, Antony K, Showalter L, Sharma S, Haymond M, Aagaard KM. Candy twists as an alternative to the glucola beverage in gestational diabetes mellitus screening. Am J Obstet Gynecol. 2015;212(4):522.e1–522.e5225. doi: 10.1016/j.ajog.2014.11.010.
- Posner NA, Silverstone FA, Breuer J, Heller M. Simplifying the intravenous glucose tolerance test. J Reprod Med. 1982;27(10):633–638. Available at: https://pubmed.ncbi.nlm.nih.gov/.
- Ardilouze A, Bouchard P, Hivert MF, Simard C, Allard C, Garant MP et al. Self-Monitoring of Blood Glucose: A Complementary Method Beyond the Oral Glucose Tolerance Test to Identify Hyperglycemia During Pregnancy. Can J Diabetes. 2019;43(8):627–635. doi: 10.1016/j.jcjd.2019.02.004.
- Иванов АС, Малин АА. Композиция для определения толерантности к глюкозе у беременных. Патент RU 2 784 241 C1. 21.03.2022. Режим доступа: https://patenton.ru/.
Фото:
Shutterstoсk/FOTODOM



 1
1 2
2 3
3 4
4


Комментарии (0)