Клинический случай
Когда медикаментозная терапия при доброкачественной гиперплазии предстательной железы перестает работать, следующий шаг обычно очевиден – хирургия. Но вместе с ней приходят и риски: кровотечения, сексуальная дисфункция, осложнения, которых пациент нередко боится не меньше самой болезни. А что если есть альтернатива – менее травматичная, но требующая высокой точности?
Урология Клинический случай ДГПЖ Журнальная публикация
О чём статья
В статье разбирается клинический случай, в котором исход лечения во многом зависел не только от выбора метода, но и от того, насколько точно врач «видит» сосудистую анатомию. Современные технологии визуализации здесь становятся не дополнением, а ключевым инструментом успеха.
Из статьи вы узнаете:
- почему эмболизация простатических артерий рассматривается как альтернатива хирургическому лечению ДГПЖ;
- в чем заключаются основные преимущества метода ЭПА по сравнению с ТУРП и открытой простатэктомией;
- какие осложнения традиционного хирургического лечения стимулируют поиск малоинвазивных подходов;
- как проходит процедура эмболизации простатических артерий на практике – от доступа до окклюзии сосудов;
- какую роль играет трансрадиальный доступ и в чем его преимущества перед трансфеморальным;
- почему сосудистая анатомия малого таза становится главным техническим вызовом при ЭПА;
- какие риски связаны с нецелевой эмболизацией и как их минимизировать;
- какие результаты удалось получить у пациента с длительно неэффективной медикаментозной терапией;
- чем объясняется высокая безопасность и хорошая переносимость метода;
- почему развитие методов визуализации становится ключевым фактором повышения эффективности эндоваскулярных вмешательств.
Журнал: «Медицинский совет» №23/2025
DOI: 10.21518/ms2025-550
Фото: Medical Art Inc/FOTODOM/Shutterstoсk
Авторы
Б.М. Шарафутдинов1,2,3, ORCID: 0000-0002-4149-118X
Т.Х. Хайруллин3, ORCID: 0009-0005-3064-9593
1 Российская медицинская академия непрерывного профессионального образования; 125993, Россия, Москва, ул. Баррикадная, д. 2/1, стр. 1
2 Казанская государственная медицинская академия; 420012, Россия, Казань, ул. Бутлерова, д. 36
3 Республиканский клинический онкологический диспансер имени профессора М.З. Сигала; 420029, Россия, Казань, ул. Сибирский тракт, д. 29
Аннотация
В статье представлен клинический случай пациента 50 лет с доброкачественной гиперплазией предстательной железы 2-й стадии и острой задержкой мочи. В течение почти трех лет он испытывал симптомы со стороны нижних мочевыводящих путей и проходил медикаментозное лечение без каких-либо клинических улучшений. Пациенту проведена эмболизация простатических артерий с применением цифровых технологий наложения визуализации для детального определения сосудистой анатомии малого таза и верификации простатических артерий. Доброкачественная гиперплазия предстательной железы (ДГПЖ) – одно из самых распространенных доброкачественных урологических заболеваний полиэтиологической природы у мужчин, приводящих к обструкции нижних мочевыводящих путей. Из-за интра- и послеоперационных осложнений, связанных с хирургическими методами лечения ДГПЖ, таких как кровотечение, инфекция, ТУР-синдром (осложнение трансуретральной резекции), недержание мочи, стриктура уретры, эректильная дисфункция, ретроградная эякуляция, возрос интерес к менее инвазивным вмешательствам. В отличие от хирургического лечения, эмболизация простатических артерий (ЭПА) имеет преимущества, заключающиеся в минимальной инвазивности процедуры с коротким периодом госпитализации и ранней активизацией, с низким риском серьезных осложнений. Однако процедура сопряжена с техническими трудностями в связи со сложной анатомией сосудов малого таза. С целью точной идентификации простатических артерий и предотвращения риска развития осложнений при планировании оперативного вмешательства оптимально применять высокоточные методы визуализации, позволяющие максимально детально оценить сосудистую анатомию и улучшить прогноз вмешательства.
Для цитирования: Шарафутдинов БМ, Хайруллин ТХ. Суперселективная катетеризация простатических артерий при проведении рентгенэндоваскулярного метода лечения доброкачественной гиперплазии предстательной железы: описание клинического случая. Медицинский совет. 2025;19(23):188–195. https://doi.org/10.21518/ms2025-550.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Благодарности. Исследование выполнено за счет гранта Академии наук Республики Татарстан, предоставленного молодым кандидатам наук (постдокторантам) с целью защиты докторской диссертации, выполнения научно-исследовательских работ, а также выполнения трудовых функций в научных и образовательных организациях Республики Татарстан.
Согласие пациента на публикацию: пациент подписал информированное согласие на публикацию своих данных.
Superselective catheterization of the prostatic arteries during X-ray endovascular treatment of benign prostatic hyperplasia: A clinical case report
Bulat M. Sharafutdinov1,2,3, ORCID: 0000-0002-4149-118X
Timur Kh. Khairullin3, ORCID: 0009-0005-3064-9593
1 Russian Medical Academy of Postgraduate Education; 2/1, Bldg. 1, Barrikadnaya St., Moscow, 125993, Russia
2 Kazan State Medical Academy; 36, Butlerov St., Kazan, 420012, Russia
3 Republican Clinical Oncological Dispansery named after Professor M.Z. Sigal; 29, Sibirskiy Tract St., Kazan, 420029, Russia
The article presents the clinical case of a 50-year-old patient with stage 2 benign prostatic hyperplasia and acute urinary retention. He had been experiencing lower urinary tract symptoms for almost three years and was undergoing medication without any clinical improvement. The patient underwent embolization of the prostatic arteries using digital imaging technologies for detailed determination of the vascular anatomy of the pelvis and verification of the prostatic arteries. Benign prostatic hyperplasia (BPH) is one of the most common benign urological diseases of a polyetiological nature in men, leading to obstruction of the lower urinary tract. Due to intra- and postoperative complications associated with surgical treatment of BPH, such as bleeding, infection, TUR syndrome (a complication of transurethral resection), urinary incontinence, urethral stricture, erectile dysfunction, and retrograde ejaculation, there has been an increased interest in less invasive interventions. Unlike surgical treatment, prostatic artery embolization (PAE) has the advantage of being a minimally invasive procedure with a short hospital stay and early mobilization, and a low risk of serious complications. However, the procedure is technically challenging due to the complex anatomy of the pelvic vessels. To accurately identify the prostatic arteries and minimize the risk of complications, it is optimal to use high-resolution imaging techniques to assess the vascular anatomy in detail and improve the outcome of the procedure.
For citation: Sharafutdinov ВМ, Khairullin TKh. Superselective catheterization of the prostatic arteries during X-ray endovascular treatment of benign prostatic hyperplasia: A clinical case report. Meditsinskiy Sovet. 2025;19(23):188–195. (In Russ.) https://doi.org/10.21518/ms2025-550.
Conflict of interest: the authors declare no conflict of interest.
Acknowledgments. The study was funded by the Tatarstan Academy of Sciences grant, which was provided to young candidates of science (postdoctorants) for the defense of doctorates, performance of research, and fulfilment of work obligations in scientific and educational organizations of the Republic of Tatarstan.
Basic patient privacy consent: patient signed informed consent regarding publishing his data.
Введение
Доброкачественная гиперплазия предстательной железы (ДГПЖ) – одно из самых распространенных доброкачественных урологических заболеваний полиэтиологической природы у мужчин, возникающее вследствие разрастания периуретральной железистой зоны предстательной железы и приводящее к доброкачественному увеличению предстательной железы, доброкачественной простатической обструкции и/или симптомам нижних мочевых путей (СНМП).
Медикаментозное лечение ДГПЖ средней и тяжелой степени включает в себя блокаторы α-адренорецепторов, ингибиторы 5-α-редуктазы, антагонисты мускариновых рецепторов и ингибиторы фосфодиэстеразы.
Хирургия предстательной железы показана пациентам с медикаментозными рефрактерными СНМП при ДГПЖ. Трансуретральная резекция простаты (ТУРП) считается золотым хирургическим стандартом для мужчин с легким или умеренным увеличением простаты. Открытая аденомэктомия (чреспузырная, позадилонная, промежностная) (ОА) описана более 100 лет назад и по-прежнему актуальна у пациентов с большим объемом предстательной железы [1].
Из-за интра- и послеоперационных осложнений, связанных с ТУРП и ОА, таких как кровотечение, инфекция, ТУР-синдром, недержание мочи, стриктура уретры, эректильная дисфункция, ретроградная эякуляция, возрос интерес к менее инвазивным вмешательствам. Вместо ТУРП были предложены такие альтернативные варианты, как фотоселективная вапоризация простаты, трансуретральная игольчатая абляция, трансуретральная инцизия простаты, трансуретральная микроволновая терапия и простатический уретральный лифтинг. Особое место среди малоинвазиных методов лечения занимает эмболизация простатических артерий (ЭПА) [2, 3].
ЭПА была предложена в качестве безопасной и эффективной альтернативы облегчению симптомов нижних мочевых путей, вторичных по отношению к доброкачественной гиперплазии предстательной железы. В отличие от хирургического лечения, ЭПА имеет преимущества, заключающиеся в минимальной инвазивности амбулаторной процедуры с коротким периодом госпитализации и ранней активизацией, с низким риском серьезных осложнений. ЭПА достигает своего терапевтического эффекта за счет индукции ишемического некроза и уменьшения объема предстательной железы, а также снижения нервно-мышечного тонуса. Иная точка приложения воздействия, а именно блокирование артериального кровотока узла гиперплазии, и, как следствие, его дальнейшая редукция, позволяет выполнять вмешательства без использования методов анестезиологического пособия, что делает возможность его применения у более широкой группы нуждающихся пациентов. Имеющиеся данные показывают многообещающие результаты, однако необходимы дальнейшие исследования для определения ЭПА как части стандартного алгоритма лечения пациентов с СНМП/ДГПЖ [4].
Клинический случай
В данном сообщении демонстрируем клинический случай эмболизации простатических артерий у пациента с доброкачественной гиперплазией предстательной железы с применением технологий наложения цифровой визуализации для детального определения сосудистой анатомии малого таза и верификации простатических артерий.
Пациент 50 лет поступил в урологическое отделение с доброкачественной гиперплазией предстательной железы 2-й стадии и острой задержкой мочи, был направлен на процедуру эмболизации простатических артерий. В течение почти трех лет он испытывал симптомы со стороны нижних мочевыводящих путей и проходил медикаментозное лечение без каких-либо клинических улучшений. Из сопутствующих заболеваний имеются гипертоническая болезнь 2-й стадии и ожирение 1-й степени. По данным трансректального ультразвукового исследования предстательной железы, размеры предстательной железы составляли 6,86 х 6,7 х 6,32 см, объем – 151 см3, с ровными контурами, неоднородной структуры. В связи с возможными рисками развития интра- и послеоперационных осложнений, связанных с ТУРП и ОА, такие как ретроградная эякуляция, для сохранения репродуктивной функции пациенту была предложена малоинвазивная альтернативная методика лечения ДГПЖ – рентгенэндоваскулярная эмболизация простатических артерий.
Процедура рентгенэндоваскулярной эмболизации простатических артерий была выполнена на ангиографическом комплексе Siemens Artis Q с программным обеспечением syngo X Workplace VD10 и возможностью проведения ротационной 3D-ангиографии с синхронизацией инъекционной системы для введения контраста. Ангиографические изображения были оценены на предмет верификации артерий таза, простатических артерий и выбора оптимальной проекции для селективной катетеризации простатических артерий при проведения ротационной 3D-ангиографии. Доступ осуществлялся через правую лучевую артерию через интродьюсер 16 см 5F. По диагностическому проводнику 0,035 позиционировался диагностический катетер Pigtail 5F над бифуркацией устьев обеих общих подвздошных артерий. С помощью ангиографического протокола 6s DCT Body был выбран режим введения контрастного вещества через инъекционную систему: скорость – 5 мл/с, общий объем – 50 мл, продолжительностью введения – 13 сек, с задержкой рентгеновского излучения – 7 сек. Далее с помощью программы syngo Embolization Guidance были отмечены точки в дистальном сегменте простатической артерии и в проксимальном сегменте внутренней подвздошной артерии (рис. 1).
Рисунок 1. Программа syngo Embolization Guidance – цифровая программа определения и визуализации правой простатической артерии, питающей аденому простаты до эмболизации
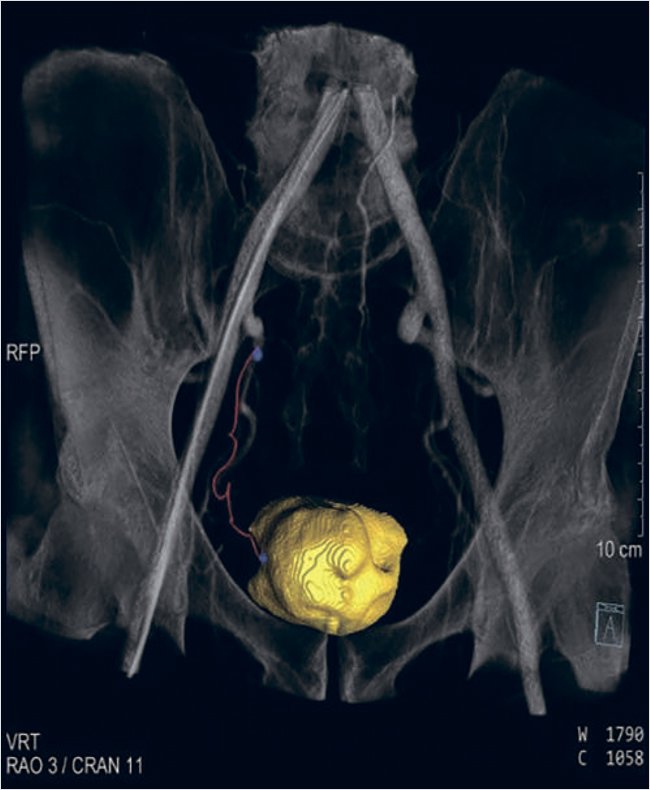
При запуске программы автоматически создается цифровая маркерная дорожка между двумя точками, которая была наложена на флюорографические изображения органов малого таза в режиме реального времени (рис. 2, 4).
Рисунок 2. Селективная катетеризация простатической артерии справа. Ангиография простатической артерии справа до эмболизации
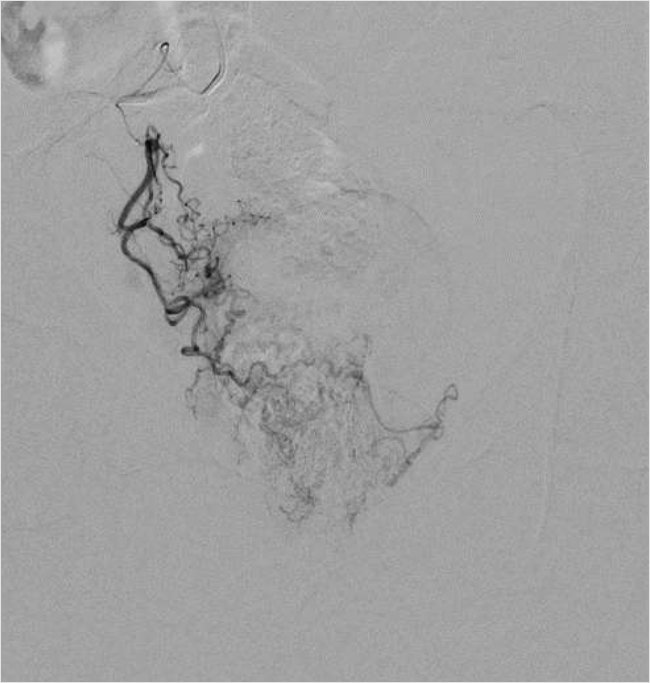
Рисунок 4. Селективная катетеризация простатической артерии слева. Ангиография простатической артерии слева до эмболизации
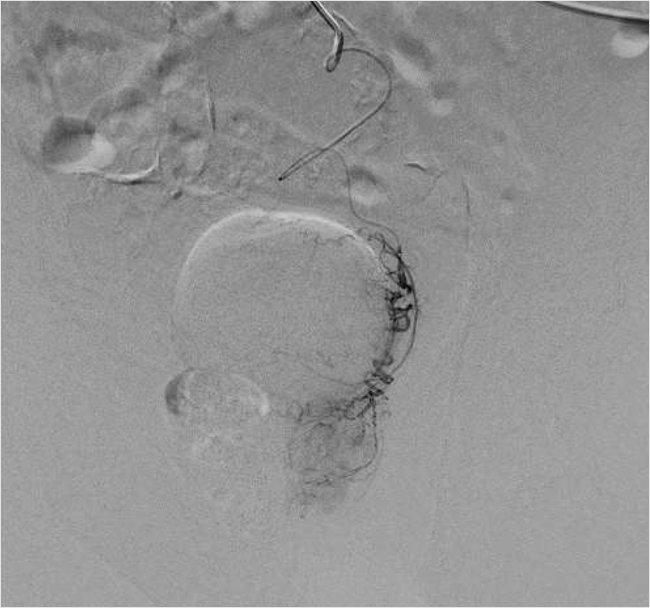
Для катетеризации простатических артерий по диагностическому проводнику был заменен катетер на диагностический гидрофильный катетер Terumo 4F длиной 150 см и микрокатетер Progreat Lambda 1,9F длиной 175 см с интервенционным гидрофильным проводником 0,014. Микрокатетер избирательно по интервенционному проводнику был поэтапно позиционирован в правой и левой простатической артерии (рис. 3, 5).
Рисунок 3. Программа syngo Embolization Guidance – цифровая программа определения и визуализации левой простатической артерии, питающей аденому простаты до эмболизации
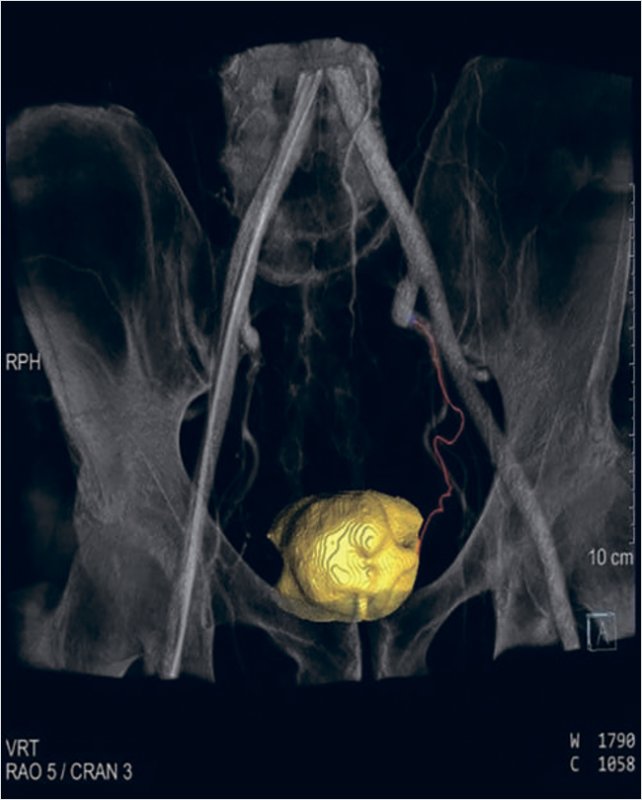
Рисунок 5. Ангиография простатической артерии справа после эмболизации
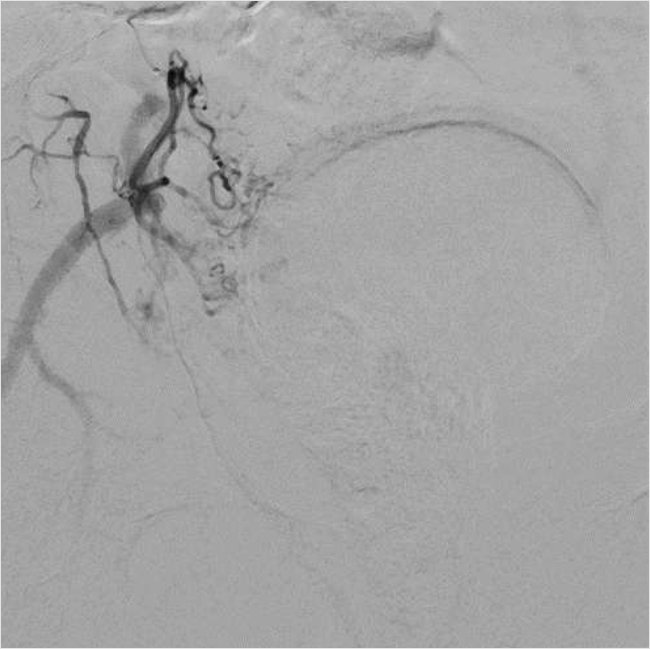
Затем была выполнена успешная окклюзия артерий с использованием микросфер (размером 100–300 мкм) до полного стаза контраста в дистальных сегментах простатических артерий (рис. 6). Дополнительных источников кровоснабжения простаты не было выявлено. Время вмешательства составило 75 мин. Доза лучевой нагрузки при проведении вмешательства составила 871 mGy. Объем введенного контрастного препарата равнялся 150 мл.
Рисунок 6. Ангиография простатической артерии слева после эмболизации
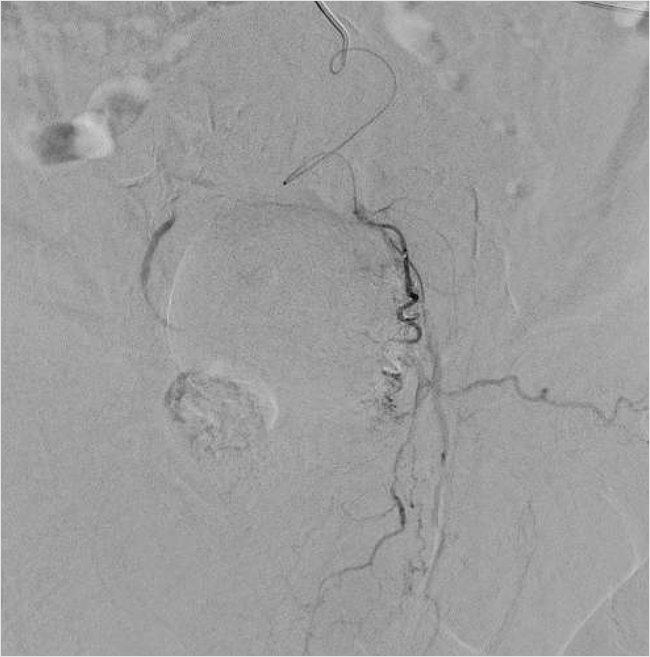
Ранний послеоперационный период протекал гладко, без осложнений. Ультразвуковое исследование простаты, выполненное на 3-и сут. после вмешательства, подтвердило отсутствие кровотока в аденоме простаты, размер и объем предстательной железы уменьшился.
Размер предстательной железы составил 6,5 х 6,33 х 6,4 см, объем – 138 см3. На 5-е сут. пациент был выписан домой с клиническим улучшением.
Обсуждение
Описанный случай рентгенэндоваскулярной эмболизации простатических артерий у пациента с доброкачественной гиперплазией предстательной железы с применением цифровых технологий наложения визуализации для детального определения сосудистой анатомии малого таза и верификации простатических артерий показывает эффективность данной технологии. Применение технологий наложения цифровой визуализации для верификации простатических артерий при проведении рентгенэндоваскулярной эмболизации аденомы предстательной железы особенно важно при сложных анатомических извитостях подвздошных артерий, позволяет улучшить прогноз вмешательства, минимизировав риск развития нежелательных событий.
Основным доступом для проведения большинства периферических и висцеральных эндоваскулярных вмешательств в настоящее время остается трансфеморальный. Однако трансфеморальный доступ ассоциируется с рядом существенных осложнений (постпункционная пульсирующая гематома, забрюшинное кровотечение, образование псевдоаневризм и артериовенозных фистул). В некоторых исследованиях риск возникновения осложнений, связанных с использованием трансфеморального доступа, достигал 10% [5]. Но существуют ситуации, когда использование данного доступа ограничено. К ряду таких причин следует отнести диффузный атеросклероз, кальциноз и кинкинг аортоподвздошного сегмента, а также сосудистые реконструкции на данном сегменте в анамнезе.
Альтернативными сосудистыми доступами являются трансбрахиальный и трансрадиальный. Трансрадиальный доступ для проведения коронарографии впервые был применен в 1989 г. [6], приобрел в дальнейшем широкое распространение и в настоящее время является доступом выбора при проведении чрескожных коронарных вмешательств.
Различные исследования показали преимущество трансрадиального доступа при разнотипных периферических вмешательствах [7], в частности эмболизации маточных [8] и простатических артерий, химиоэмболизации печени [9], в которых сообщается низкий уровень осложнений и высокий процент технического успеха процедуры. Кроме того, трансрадиальный доступ стал предпочтительным для большинства пациентов и был связан с меньшей лучевой нагрузкой на пациентов и медицинский персонал и сокращением времени вмешательства [10, 11].
История развития метода ЭПА началась с 1992 г., когда Mitchell et al. впервые сообщили о четырех случаях успешного применения двусторонней транскатетерной артериальной эмболизации внутренних подвздошных артерий для лечения тяжелой гематурии. Метод зарекомендовал себя как безопасный и эффективный способ остановки жизнеугрожающих кровотечений из мочевого пузыря или простаты, когда традиционные методы лечения не дали результата. С развитием технологий, в частности появления микрокатетеров, техника проведения процедуры значительно усовершенствовалась: от неселективной эмболизации внутренней подвздошной артерии к высокоселективной катетеризации ее ветвей [12].
В 2000 г. J.S. DeMeritt et al. продемонстрировали удовлетворительные отдаленные результаты эмболизации нижнепузырной артерии частицами поливинилалкоголя у пациента с гематурией, не купирующейся консервативными методами [13].
Первые успешные случаи ЭПА у пациентов с острой задержкой мочи, связанной с ДГПЖ, были описаны F.C. Carnevale et al. в 2010 г. [14]. Благодаря последующему активному использованию ЭПА у пациентов с высоким риском традиционных хирургических вмешательств на простате, в т. ч. при гигантских размерах железы, можно было сделать вывод, что данный метод обладает исключительной эффективностью в устранении клинических проявлений СНМП у пациентов, ранее считавшихся неоперабельными [15–18].
Группа авторов во главе с J.M. Pisco в 2011 и 2013 гг. опубликовали серию случаев проведения ЭПА у пациентов с СНМП. Технический успех процедуры составил 71,4%. В послеоперационном периоде наблюдалось значимое снижение IPSS, улучшение качества жизни, увеличение максимальной скорости потока мочи (по данным урофлоуметрии) и снижение объема простаты. Зарегистрировано одно серьезное осложнение в виде ишемии мочевого пузыря, потребовавшее в дальнейшем хирургического вмешательства [19–22].
Согласно данным систематического обзора V. Zumstein et al., ЭПА оказалась менее эффективной в отношении улучшения всех оцениваемых функциональных параметров, включая максимальный поток мочи, остаточную жидкость после мочеиспускания и уменьшение объема простаты. Напротив, отмечено преимущество ЭПА в плане сохранения/улучшения эректильной функции, по оценкам пациентов (Международный индекс эректильной функции – 5), и частоты побочных эффектов [23].
B. Moulin et al. в публикации 2022 г. отмечали эффективность метода в отношении как симптомов мочеиспускания, так и флоуметрических параметров. Основным преимуществом данной процедуры является крайне низкая частота мочевых и сексуальных осложнений, включая недержание мочи, ретроградную эякуляцию и эректильную дисфункцию, а также хорошую переносимость по сравнению с традиционными хирургическими методами [24, 25]. Ключевым фактором успешной эмболизации является знание сосудистой анатомии малого таза, которое позволяет предотвратить потенциальные осложнения, связанные с нецелевой эмболизацией, такие как некроз мочевого пузыря, прямой кишки, головки полового члена, кожи ягодичной области. Нецелевая эмболизация может быть выполнена при рефлюксе либо наличии анастомозов простатической артерии с другими ветвями внутренней подвздошной артерии (мочепузырные, внутренняя половая, прямокишечные, запирательная и другие артерии) [26].
Сосудистая анатомия малого таза весьма вариабельна, имеет крайне сложную анатомию и коллатеральное кровообращение, а также анастомозы простатических артерий с другими ветвями внутренних подвздошных артерий. Этим объясняется техническая сложность идентификации и селективной катетеризации простатических артерий, а также риск нецелевой эмболизации и связанных с ней последствий, что влияет на эффективность и безопасность процедуры [27, 28].
В метаанализе Xu. Zhunan et al. отмечено, что уменьшение объема предстательной железы и увеличение максимальной скорости потока при свободной урофлоуметрии оказались более достижимы при ТУРП, чем при ЭПА; однако частота сексуальной дисфункции была ниже при ЭПА. Между тем не было выявлено заметной разницы в показателях Международной шкалы симптомов заболеваний простаты (IPSS), качества жизни (Qol), остаточного объема мочи, простат-специфического антигена и осложнений между двумя группами [29].
Данные метаанализа R. Altman et al. 2024 г. продемонстрировали, что ТУРП и открытая простатэктомия (ОП) были связаны со статистически более значимым улучшением уродинамических показателей и симптомов ДГПЖ по сравнению с ЭПА. Тем не менее ЭПА значительно улучшает эректильную функцию по сравнению с ОП и улучшает другие показатели эффективности по сравнению с ТУРП, а также сопровождается более низкой частотой побочных эффектов и приводит к меньшему количеству незначительных осложнений по сравнению с ТУРП и ОП [30].
Ввиду особенностей ангиоархитектоники малого таза с целью повышения эффективности и безопасности процедуры эмболизации применяются высокоточные методы визуализации сосудов малого таза, позволяющие максимально детально оценить сосудистую анатомию и улучшить прогноз вмешательства.
В исследовании 2017 г. M.Q. Wang et al. пришли к выводу, что конусно-лучевая компьютерная томография является полезным дополнительным методом к цифровой субтракционной ангиографии (DSA). Конусно-лучевая компьютерная томография позволила идентифицировать простатические артерии у 100% пациентов, а также обнаружить анастомозы с другими сосудами малого таза, что было недоступно при DSA у 60,8% пациентов [31]. Также ряд исследований доказывает пользу данного метода при планировании оперативного вмешательства [32–35].
В сообщении В.П. Климова и соавт. описано неотъемлемое преимущество применения ротационной плоскопанельной ангиографии с возможностью 3D-реконструкции по полученным изображениям. В серии из 7 клинических случаев продемонстрирована детальная визуализация сосудистых структур различных локализаций. Внедрение данных методов визуализации в рутинную практику облегчит идентификацию и селективную катетеризацию целевых сосудов, сократит время вмешательства, а также снизит риск потенциальных осложнений [36].
Таким образом, рентгенэндоваскулярный метод лечения ДГПЖ является актуальным, т. к. осложнения от хирургического лечения остаются высокими и методы органосохраняющего лечения требуют дальнейшей оптимизации подходов в визуализации простатических артерий [37].
Заключение
Таким образом, клинический случай показал эффективность рентгенэндоваскулярной эмболизации простатических артерий у пациента с доброкачественной гиперплазией предстательной железы и острой задержкой мочи с применением цифровых технологий наложения визуализации для детального определения сосудистой анатомии малого таза и верификации простатических артерий.
Рентгенэндоваскулярная эмболизация простатических артерий – это перспективный органосохраняющий метод, обладающий высоким профилем эффективности и безопасности и позволяющий с минимальной травматичностью достичь уменьшения аденомы предстательной железы. Однако в связи со сложной анатомией сосудов малого таза процедура сопряжена с определенными техническими трудностями. С целью дифференциации сосудистых структур и идентификации простатических артерий применяются высокоточные методы визуализации, в частности создание цифровой маркерной дорожки, позволяющие при выполнении оперативного вмешательства максимально детально оценить сосудистую анатомию малого таза, осуществить суперселективную катетеризацию артерий предстательной железы и тем самым улучшить прогноз вмешательства, минимизировав риск развития нежелательных событий.
Применение технологий наложения цифровой визуализации для верификации простатических артерий при проведении рентгенэндоваскулярной эмболизации доброкачественной гиперплазии предстательной железы позволяет в клинической практике снижать время вмешательства и лучевую нагрузку на пациента и медицинский персонал, что особенно важно при сложных анатомических извитостях подвздошных артерий. Также использование системы помощи визуализации целевой артерии на ангиографических системах последнего поколения позволяет рентгенэндоваскулярным хирургам более точно манипулировать проводниками и катетерами, ориентируясь в сосудах для более точного и быстрого проведения избирательной эмболизации целевой артерии, тем самым снижая риск неполноценной эмболизации. При проведении ЭПА в таком режиме увеличивается процент верификации простатических артерий и визуализируются наиболее оптимальные проекции для повышения эффективности рентгенэндоваскулярного вмешательства, что положительно скажется на повышении качества жизни и репродуктивном здоровье мужского населения.
Список литературы / References
Развернуть
- Лопаткин НА (ред.). Урология. М.: ГЭОТАР-Медиа; 2013. 1024 с.
- Russo GI, Kurbatov D, Sansalone S, Lepetukhin A, Dubsky S, Sitkin I et al. Prostatic Arterial Embolization vs Open Prostatectomy: A 1-Year Matched-pair Analysis of Functional Outcomes and Morbidities. Urology. 2015;86(2):343–348. doi: 10.1016/j.urology.2015.04.037.
- Abt D, Hechelhammer L, Müllhaupt G, Markart S, Güsewell S, Kessler TM et al. Comparison of prostatic artery embolisation (PAE) versus transurethral resection of the prostate (TURP) for benign prostatic hyperplasia: randomised, open label, non-inferiority trial. BMJ. 2018;361:k2338. doi: 10.1136/bmj.k2338.
- Cui L, Bai Y, Zhang J, Yuan B, Wang X, Wang Y et al. Prostatic artery embolization: Progress and prospect. J Interv Med. 2020;3(2):77–79. doi: 10.1016/j.jimed.2020.03.003.
- Kiemeneij F, Laarman GJ. Percutaneous transradial artery approach for coronary stent implantation. Cathet Cardiovasc Diagn. 1993;30(2):173–178. doi: 10.1002/ccd.1810300220.
- Campeau L. Percutaneous radial artery approach for coronary angiography. Cathet Cardiovasc Diagn. 1989;16(1):3–7. doi: 10.1002/ccd.1810160103.
- Thakor AS, Alshammari MT, Liu DM, Chung J, Ho SGF, Legiehn GM et al. Transradial Access for Interventional Radiology: Single-Centre Procedural and Clinical Outcome Analysis. Can Assoc Radiol J. 2017;68(3):318–327. doi: 10.1016/j.carj.2016.09.003.
- Resnick NJ, Kim E, Patel RS, Lookstein RA, Nowakowski FS, Fischman AM. Uterine artery embolization using a transradial approach: initial experience and technique. J Vasc Interv Radiol. 2014;25(3):443–447. doi: 10.1016/j.jvir.2013.11.010.
- Хайрутдинов ЕР, Громов ДГ, Араблинский АВ, Воронцов ИМ, Леонов ОВ, Кальченко ЕА, Игнатьев ЮТ. Применение трансрадиального и трансфеморального доступов при химиоэмболизации печеночной артерии в лечении больных злокачественными новообразованиями печени. Уральский медицинский журнал. 2023;22(5):77–86. doi: 10.52420/2071-5943-2023-22-5-77-86. / Khayrutdinov ER, Gromov DG, Arablinskiy AV, Vorontsov IM, Leonov OV, Kalchenko EA, Ignatev YT. Application of transradial and transfemoral accesses during hepatic artery chemoembolization in the treatment of patients with malignant liver neoplasms. Ural Medical Journal. 2023;22(5):77–86. (In Russ.) doi: 10.52420/2071-5943-2023-22-5-77-86.
- Хайрутдинов ЕР, Воронцов ИМ, Жариков СБ, Араблинский АВ, Игнатьев ЮТ, Леонов ОВ. Преимущества трансрадиального сосудистого доступа при эмболизации простатических артерий. Российский онкологический журнал. 2017;22(2):84–88. doi: 10.18821/1028-9984-2017-22-2-84-88. / Khayrutdinov ER, Vorontsov IM, Zharikov SB, Arablinskiy AV, Ignatiev YT, Leonov OV. The advantage of the transradial approach for prostate artery embolization. Russian Journal of Oncology. 2017;22(2):84–88. (In Russ.) doi: 10.18821/1028-9984-2017-22-2-84-88.
- Stavroulakis K, Usai MV, Torsello G, Schwindt A, Stachmann A, Beropoulis E, Bisdas T. Efficacy and Safety of Transbrachial Access for Iliac Endovascular Interventions. J Endovasc Ther. 2016;23(3):454–460. doi: 10.1177/1526602816640522.
- Bilhim T, Casal D, Furtado A, Pais D, O’Neill JE, Pisco JM. Branching patterns of the male internal iliac artery: imaging findings. Surg Radiol Anat. 2011;33(2):151–159. doi: 10.1007/s00276-010-0716-3.
- DeMeritt JS, Elmasri FF, Esposito MP, Rosenberg GS. Relief of benign prostatic hyperplasia-related bladder outlet obstruction after transarterial polyvinyl alcohol prostate embolization. J Vasc Interv Radiol. 2000;11(6):767–770. doi: 10.1016/s1051-0443(07)61638-8.
- Carnevale FC, Antunes AA, da Motta Leal Filho JM, de Oliveira Cerri LM, Baroni RH, Marcelino AS et al. Prostatic artery embolization as a primary treatment for benign prostatic hyperplasia: preliminary results in two patients. Cardiovasc Intervent Radiol. 2010;33(2):355–361. doi: 10.1007/s00270-009-9727-z.
- Carnevale FC, da Motta-Leal-Filho JM, Antunes AA, Baroni RH, Marcelino AS, Cerri LM et al. Quality of life and clinical symptom improvement support prostatic artery embolization for patients with acute urinary retention caused by benign prostatic hyperplasia. J Vasc Interv Radiol. 2013;24(4):535–542. doi: 10.1016/j.jvir.2012.12.019.
- Carnevale FC, Iscaife A, Yoshinaga EM, Moreira AM, Antunes AA, Srougi M. Transurethral Resection of the Prostate (TURP) Versus Original and PErFecTED Prostate Artery Embolization (PAE) Due to Benign Prostatic Hyperplasia (BPH): Preliminary Results of a Single Center, Prospective, Urodynamic-Controlled Analysis. Cardiovasc Intervent Radiol. 2016;39(1):44–52. doi: 10.1007/s00270-015-1202-4.
- Carnevale FC, Antunes AA. Prostatic artery embolization for enlarged prostates due to benign prostatic hyperplasia. How I do it. Cardiovasc Intervent Radiol. 2013;36(6):1452–1463. doi: 10.1007/s00270-013-0680-5.
- Delazar S, Azadnajafabad S, Firouznia K, Nowroozi MR, Amini E, Fotouhi M, Ghanaati H. Outcomes of Prostatic Artery Embolization for Treating Benign Prostatic Hyperplasia Symptoms: A Prospective Single-Center Study. Health Sci Rep. 2025;8(3):e70565. doi: 10.1002/hsr2.70565.
- Pisco JM, Pinheiro LC, Bilhim T, Duarte M, Mendes JR, Oliveira AG. Prostatic arterial embolization to treat benign prostatic hyperplasia. J Vasc Interv Radiol. 2011;22(1):11–19. doi: 10.1016/j.jvir.2010.09.030.
- Pisco J, Campos Pinheiro L, Bilhim T, Duarte M, Rio Tinto H, Fernandes L et al. Prostatic arterial embolization for benign prostatic hyperplasia: short- and intermediate-term results. Radiology. 2013;266(2):668–677. doi: 10.1148/radiol.12111601.
- Pisco JM, Bilhim T, Pinheiro LC, Fernandes L, Pereira J, Costa NV et al. Medium- and Long-Term Outcome of Prostate Artery Embolization for Patients with Benign Prostatic Hyperplasia: Results in 630 Patients. J Vasc Interv Radiol. 2016;27(8):1115–1122. doi: 10.1016/j.jvir.2016.04.001.
- Christidis D, Clarebrough E, Ly V, Perera M, Woo H, Lawrentschuk N, Bolton D. Prostatic artery embolization for benign prostatic obstruction: assessment of safety and efficacy. World J Urol. 2018;36(4):575–584. doi: 10.1007/s00345-018-2220-z.
- Zumstein V, Betschart P, Vetterlein MW, Kluth LA, Hechelhammer L, Mordasini L et al. Prostatic Artery Embolization versus Standard Surgical Treatment for Lower Urinary Tract Symptoms Secondary to Benign Prostatic Hyperplasia: A Systematic Review and Meta-analysis. Eur Urol Focus. 2019;5(6):1091–1100. doi: 10.1016/j.euf.2018.09.005.
- Moulin B, Di Primio M, Vignaux O, Sarrazin JL, Angelopoulos G, Hakime A. Prostate Artery Embolization: Challenges, Tips, Tricks, and Perspectives. J Pers Med. 2022;13(1):87. doi: 10.3390/jpm13010087.
- Жариков СБ, Рослик СС, Цымбал ЕВ, Иванов ВА, Кочетов АГ, Есипов АВ и др. Непосредственные и отдаленные результаты эмболизации простатических артерий у больных с доброкачественной гиперплазией простаты высокого хирургического и анестезиологического риска. Вестник Российского университета дружбы народов. Серия: Медицина. 2017;21(2):270–280. doi: 10.22363/2313-0245-2017-21-2-270-280. / Zharikov SB, Roslik SS, Tsymbal EV, Ivanov VA, Kochetov AG, Esipov AV et al. Short- and long-term outcomes of selective prostatic artery embolization in patient high surgical and anestesilogical risk. RUDN Journal of Medicine. 2017;21(2):270–280. (In Russ.) doi: 10.22363/2313-0245-2017-21-2-270-280.
- Khunte M, Gaupp FML. Anatomy for Prostatic Artery Embolization. Semin Intervent Radiol. 2025;42(2):213–218. doi: 10.1055/s-0045-1804908.
- Șerbănoiu A, Nechifor R, Marinescu AN, Iana G, Bratu AM, Sălcianu IA et al. Prostatic Artery Origin Variability: Five Steps to Improve Identification during Percutaneous Embolization. Medicina. 2023;59(12):2122. doi: 10.3390/medicina59122122.
- Капранов СА, Златовратский АГ, Карпов ВК, Шапаров БМ, Камалов АА. Варианты кровоснабжения простаты при выполнении суперселективной эмболизации простатических артерий. Вестник урологии. 2021;9(3):32–43. doi: 10.21886/2308-6424-2021-9-3-32-43. / Kapranov SA, Zlatovratsky AG, Karpov VK, Shaparov BM, Kamalov AA. Types of the prostate blood supply during super-selective embolization of prostatic arteries. Vestnik Urologii. 2021;9(3):32–43. (In Russ.) doi: 10.21886/2308-6424-2021-9-3-32-43.
- Xu Z, Zhou Z, Mu Y, Cai T, Gao Z, Liu L. An Updated Meta-Analysis of the Efficacy and Safety of Prostatic Artery Embolization vs. Transurethral Resection of the Prostate in the Treatment of Benign Prostatic Hyperplasia. Front Surg. 2021;8:779571. doi: 10.3389/fsurg.2021.779571.
- Altman R, Ferreira R, Barragan C, Bhojani N, Lajkosz K, Zorn KC et al. Comparing prostatic artery embolization to surgical and minimally invasive procedures for the treatment of benign prostatic hyperplasia: a systematic review and meta-analysis. BMC Urol. 2024;24(1):22. doi: 10.1186/s12894-023-01397-1.
- Wang MQ, Duan F, Yuan K, Zhang GD, Yan J, Wang Y. Benign Prostatic Hyperplasia: Cone-Beam CT in Conjunction with DSA for Identifying Prostatic Arterial Anatomy. Radiology. 2017;282(1):271–280. doi: 10.1148/radiol.2016152415.
- Rostambeigi N, Crawford D, Golzarian J. Benefits and advances of Cone Beam CT use in prostatic artery embolization: review of the literature and pictorial essay. CVIR Endovasc. 2024;7(1):46. doi: 10.1186/s42155-024-00459-1.
- Carnevale FC, McClure T, Cadour F, Vidal V, de Assis AM, Moreira AM et al. Advanced image guidance for prostatic artery embolization – a multicenter technical note. CVIR Endovasc. 2021;4(1):63. doi: 10.1186/s42155-021-00249-z.
- Скрябин ЕС, Ханалиев БВ, Масленников МА, Марчак ДИ. Эмболизация артерий предстательной железы при ее гиперплазии. Вестник Национального медико-хирургического центра им. Н.И. Пирогова. 2022;17(2):95–102. doi: 10.25881/20728255_2022_17_2_95. / Skryabin ES, Khanaliev BV, Maslennikov MA, Marchak DI. Prostatic artery embolization in benign prostatic hyperplasia. Bulletin of Pirogov National Medical & Surgical Center. 2022;17(2):95–102. (In Russ.) doi: 10.25881/20728255_2022_17_2_95.
- Dung LT, Hung ND, Thien LQ, Huyen DK, Vu LN, Hung DD, Duc NM. Dual-energy computed tomography in supporting prostatic artery embolization for benign prostatic hyperplasia. Int J Med Sci. 2024;21(9):1640–1648. doi: 10.7150/ijms.96319.
- Климов ВП, Азаров АВ, Семитко СП, Верткина НВ. Ротационная ангиография и ее роль в современной клинической практике. Consilium Medicum. 2017;19(1):42–49. Режим доступа: https://consilium.orscience.ru/. / Klimov VP, Azarov AV, Semitko SP, Vertkina NV. Rotational angiography and the role of rotational angiography in modern clinical practice. Consilium Medicum. 2017;19(1):42–49. (In Russ.) Available at: https://consilium.orscience.ru/.
- Bilhim T, Costa NV, Torres D, Pinheiro LC, Spaepen E. Long-Term Outcome of Prostatic Artery Embolization for Patients with Benign Prostatic Hyperplasia: Single-Centre Retrospective Study in 1072 Patients Over a 10-Year Period. Cardiovasc Intervent Radiol. 2022;45(9):1324–1336. doi: 10.1007/s00270-022-03199-8.
Фото:
Medical Art Inc/FOTODOM/Shutterstoсk



 1
1 2
2 3
3 4
4


Комментарии (0)