Журнал "Медицинский совет" №21/2019
DOI: 10.21518/2079-701X-2019-21-40-43
М.А. Габитова, ORCID: 0000-0003-3299-4743, e-mail: mariia_gabitova91@mail.ru
П.М. Крупенин, ORCID: 0000-0001-5203-4497, e-mail: krupeninpavel@gmail.com
А.А. Соколова, ORCID: 0000-0001-5938-8917, e-mail: sokolovastasya@rambler.ru
Д.А. Напалков, ORCID: 0000-0001-6241-2711, e-mail: dminap@mail.ru
В.В. Фомин, ORCID: 0000-0002-2682-4417, e-mail: fomin@mma.ru
Первый Московский государственный медицинский университет имени И.М. Сеченова (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2
Фибрилляция предсердий (ФП) – одна из наиболее распространенных аритмий среди пациентов в возрасте ≥75 лет. Повышение риска тромбозов в силу возраста и вследствие большого числа сопутствующих заболеваний делает очевидной необходимость назначения антикоагулянтной терапии. Однако те же самые факторы способствуют увеличению риска геморрагических осложнений, которые являются одними из самых опасных побочных эффектов антикоагулянтной терапии. Именно поэтому очень важно выявлять пациентов с наибольшей вероятностью развития кровотечений, как больших, так и небольших клинических значимых и малых. Целью нашего исследования стало изучение прогностической ценности лабораторных методов обследования в отношении развития геморрагических событий у пациентов старческого возраста с ФП, принимающих прямые оральные антикоагулянты (ПОАК). В исследование были включены 102 пациента ≥75 лет с ФП неклапанной этиологии, принимающие дабигатран, апиксабан, ривароксабан в полной или сниженной дозах. Антикоагулянты назначались врачами амбулаторного звена и стационаров. Анализировались как предшествующий опыт приема ПОАК до момента включения в исследования (если ПОАК назначались ранее), так и проспективное наблюдение за пациентами после включения в исследование. Минимальный анализируемый период приема ПОАК составил 18 месяцев. Пациенты, перенесшие (n = 19) и не перенесшие (n = 83) геморрагические события (все события были расценены как малые по критериям ISTH), не различались ни по одному из лабораторных показателей, потенциально рассматриваемых в качестве предикторов геморрагических событий.
Для цитирования: Габитова М.А., Крупенин П.М., Соколова А.А., Напалков Д.А., Фомин В.В. Лабораторные предикторы кровотечений у пациентов старческого возраста с фибрилляцией предсердий, принимающих прямые оральные антикоагулянты. Медицинский совет. 2019;(21):40-43. doi: 10.21518/2079-701X-2019-21-40-43.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Laboratory bleeding predictors in elderly patients with atrial fibrillation taking direct oral anticoagulants
Mariia A. Gabitova, ORCID: 0000-0003-3299-4743, e-mail: mariia_gabitova91@mail.ru
Pavel M. Krupenin, ORCID: 0000-0001-5203-4497, e-mail: krupeninpavel@gmail.com
Anastasiya A. Sokolova, ORCID: 0000-0001-5938-8917, e-mail: sokolovastasya@rambler.ru
Dmitriy A. Napalkov, ORCID: 0000-0001-6241-2711, e-mail: dminap@mail.ru
Viktor V. Fomin, ORCID: 0000-0002-2682-4417, e-mail: fomin@mma.ru
I.M. Sechenov First Moscow State Medical University (Sechenov University); 8-2, Trubetskaya st., Moscow, 119991, Russia
Atrial fibrillation (AF) is one of the most common arrhythmias in patients ≥75 years of age. The increased risk of thrombosis due to age and the large number of concomitant diseases makes it evident that anticoagulant therapy is necessary. However, the same factors increase the risk of hemorrhagic complications, which are among the most dangerous side effects of anticoagulant therapy. That is why it is very important to identify patients with the highest probability of bleeding, whether large or small clinically significant and minor. The purpose of our study was to study the prognostic value of laboratory methods of examination with regard to the development of hemorrhagic events in elderly patients with AF taking direct oral anticoagulants (DOAC). The study enrolled 102 patients ≥75 years of age with AF of non-valve etiology taking dabigatran, apixaban, rivaroxaban at full or reduced doses. Anticoagulants were administered by outpatient and inpatient physicians. Both previous experience with DOAC prior to inclusion in the trial (if DOAC was previously prescribed) and prospective patient monitoring after inclusion in the trial were analyzed. The minimum analyzed period of DOAC intake was 18 months. Patients who underwent (n = 19) and did not undergo (n = 83) hemorrhagic events (all events were considered small by ISTH criteria) did not differ in any of the laboratory indicators potentially considered as predictors of hemorrhagic events.
For quotation: Gabitova M.A., Krupenin P.M., Sokolova A.A., Napalkov D.A., Fomin V.V. Laboratory predictors of bleeding in elderly patients with atrial fibrillation taking direct oral anticoagulants. Meditsinskiy sovet = Medical Council. 2019;(21):40-43. (In Russ.) doi: 10.21518/2079-701X-2019-21-40-43.
Conflict of interest: the authors claim that there is no conflict of interest.
Введение
Среди всех нарушений ритма сердца ведущая роль по праву принадлежит фибрилляции предсердий (ФП) [1], и чем старше пациент, тем больше вероятность выявить у него аритмию [2, 2]. Особенно часто она встречается среди пациентов старческого возраста, то есть у лиц, достигших 75 лет. Этот факт вызывает беспокойство, поскольку, хотя ФП и не является потенциально летальным нарушением ритма, но сопутствующие ей артериальные тромбозы (главным образом ишемический инсульт) способны приводить к инвалидизации пациентов и их смерти. Как и распространенность аритмии в популяции, вероятность развития ишемического инсульта увеличивается по мере старения пациентов [4], а также при наличии ряда сопутствующих патологий (артериальная гипертензия, сахарный диабет и т.п.) [4]. Таким образом, пациентам старческого возраста необходимо своевременно назначать антикоагулянтную терапию вне зависимости от формы ФП, причем приоритет все чаще отдается прямым оральным антикоагулянтам (ПОАК), а не антагонистам витамина К [6]. Это связано не только с большей эффективностью ПОАК, но и с большей их безопасностью [7, 7].
Именно высокий риск развития кровотечений становится фактором, чаще всего осложняющим антикоагулянтную терапию у пациентов с ФП, а также служащим причиной назначения препаратов в необоснованно низких дозах или отказа от антикоагулянтной терапии [9], несмотря на то, что данные реальной клинической практики свидетельствуют о несомненном положительном эффекте применения ПОАК у пациентов старшей возрастной группы [10]. Как и в случае с риском развития тромбозов, вероятность реализации геморрагических событий возрастает по мере старения пациентов, что отражено в шкале риска развития больших кровотечений HAS-BLED [11]. Однако высокий геморрагический риск не является показанием для отмены ПОАК или назначения препарата в неадекватно низкой дозе [12]. Это всего лишь повод более тщательно осуществлять контроль за состоянием пациента, выявлять и минимизировать дополнительные факторы риска развития кровотечений.
Среди показателей лабораторных исследований, изменения которых расцениваются исследователями как предикторы кровотечений, чаще всего фигурируют показатели общего анализа крови (ОАК), в частности уровень гемоглобина (Hb) и тромбоцитов, а также показатели биохимического анализа крови: уровень креатинина плазмы и расчетная скорость клубочковой фильтрации (СКФ) [13, 14]. На основании последнего показателя диагностируется хроническая болезнь почек (ХБП), степень тяжести которой имеет прямую корреляцию с риском развития кровотечений [15]. Однако все приведенные выше данные литературы расценивают эти лабораторные показатели как значимые факторы риска кровотечения только при их критических величинах (ХБП 4-й и 5-й стадий, выраженная анемия и тромбоцитопения и т.п.), в то время как у большинства пациентов с ФП они принимают менее драматичные значения. Поэтому вопрос предсказательной значимости лабораторных данных у пациентов старческого возраста требует более тщательного изучения.
Цель. Определить прогностическую ценность лабораторных методов обследования в отношении развития геморрагических событий у пациентов старческого возраста с ФП, принимающих ПОАК.
Материалы и методы. В наше исследование включались пациенты ≥75 лет с ФП неклапанной этиологии, принимающие один из трех ПОАК – дабигатран, апиксабан или ривароксабан, в полной или сниженной дозах: 110 мг 2 раза в сутки для дабигатрана (препарат применялся только в сниженной дозировке), 5 мг 2 раза в сутки или 5 мг 2,5 раза в сутки для апиксабана, 20 мг 1 раз в сутки или 15 мг 1 раз в сутки для ривароксабана. Антикоагулянты назначались врачами амбулаторного звена и стационаров. В исследование включались только те пациенты, которые соблюдали протокол, то есть регулярно принимали ПОАК в назначенной врачом адекватной дозировке. На первом этапе анализировался ретроспективный (до момента включения в исследование) опыт приема ПОАК при его наличии. Если препарат был назначен ранее указанного возраста, мы принимали во внимание только период приема антикоагулянта с момента достижения пациентом возраста 75 лет. Ряду пациентов антикоагулянтная терапия ПОАК была впервые назначена менее чем за месяц до включения в исследование. Второй этап представлял собой проспективное наблюдение пациентов. Минимальный общий анализируемый период, включавший данные как ретро-, так и проспективного наблюдения, составил 18 месяцев для каждого пациента. В исследование не включались пациенты с клапанной этиологией ФП, обратимыми причинами нарушения ритма, а также имеющие ХБП 4-й и 5-й стадии. Оценивались риск развития ишемического инсульта по шкале CHA2DS2-VASc, риск развития кровотечения по шкале HAS-BLED, сопутствующая патология, данные лабораторных исследований (общий анализ крови, креатинин венозной плазмы и расчетная скорость клубочковой фильтрации по формуле CKD-EPI). Статистическая оценка достоверности различий между группами по параметрическим показателям проводилась при помощи t-критерия Стьюдента. За критический уровень значимости принимали р<0,05. Для оценки по непараметрическим показателям применялся критерий «хи-квадрат» (χ2) К. Пирсона (критический уровень значимости тот же).
Результаты
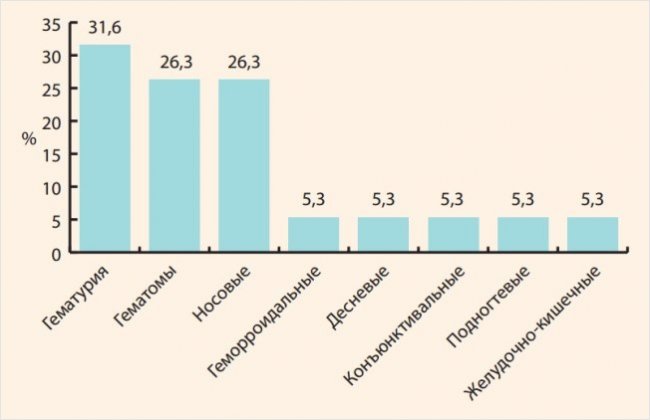
В наше исследование было включено 102 пациента (39 мужчин и 63 женщины), которые принимали один из трех ПОАК в полной или сниженной дозировках (дабигатран 110 мг 2 р/сутки; апиксабан 5 мг 2 р/сутки или 2,5 мг 2 р/сутки; ривароксабан 20 мг/сутки или 15 мг/сутки). За 18 месяцев, прошедших с момента начала терапии ПОАК (анализируемый период), на фоне проводимого лечения отмечено 19 малых кровотечений, не потребовавших отмены приема ПОАК или госпитализации. Больших кровотечений не зафиксировано. Распределение пациентов в зависимости от локализации кровотечений представлено на рисунке.
Рисунок. Структура локализации кровотечений у пациентов ≥75 лет, принимавших ПОАК (%)
Figure. Bleeding localization structure in patients ≥75 years of age who were taking DOAC (%)
По окончании проспективного периода наблюдения все пациенты были разделены на две группы: перенесшие и не перенесшие геморрагическое событие. Затем было проведено прямое сравнение пациентов в группах по лабораторным показателям, которые могут быть рассмотрены как предикторы кровотечений (табл.).
Таблица. Лабораторных характеристика пациентов ≥75 лет в зависимости от наличия геморрагических событий на приеме ПОАК
Table. Laboratory characteristics of patients ≥75 years of age depending on the presence of hemorrhagic events when receiving DOAC
Показатель
Кровотечения «+» (n = 19)
Кровотечения «–» (n = 83)
Р-достоверность
Эритроциты
4,3 ± 0,61
4,5 ± 1,22
0,58
Гемоглобин
12,7 ± 2,28
13,1 ± 1,76
0,39
Гематокрит
38,2 ± 6,68
39 ± 5,25
0,63
Тромбоциты
221,7 ± 80,77
223,6 ± 57,82
0,9
Креатинин плазмы
94,8 ± 19,65
99,5 ± 31,63
0,55
СКФ
58,2 ± 14,4
56,9 ± 16,22
0,76
HAS-BLED
2,0
1,6
0,15
Результаты исследования показали, что пациенты, перенесшие и не перенесшие геморрагические события (в нашем исследовании – малые), не различались ни по одному из показателей, потенциально рассматриваемых в качестве предикторов геморрагических событий. Мы также проанализировали показатели шкалы риска развития больших кровотечений HAS-BLED у пациентов обеих групп. Результат оказался аналогичным: группы достоверно не различались по данному критерию.
Обсуждение
Наша работа представляет собой моноцентровое проспективное нерандомизированное когортное исследование, выполненное в популяции пациентов старческого возраста и долгожителей (возрастная характеристика соответствует критериям ВОЗ). Пациенты в обеих группах имели практически идентичные значения лабораторных показателей, которые относят к вероятным предикторам кровотечений: эритроцитов, гемоглобина, гематокрита, а также креатинина плазмы и СКФ.
Все проанализированные нами показатели упоминаются в литературе в качестве маркеров геморрагических осложнений. Однако значения, которые приводятся в научной литературе, представляют собой очень резкие отклонения референтных значений, крайние степени анемии, тромбоцитопении и/или ХБП. В реальной клинической практике чаще встречаются пациенты, даже старческого возраста, у которых лабораторные показатели имеют пограничные значения или незначительно отклонены от нормы. В нашем исследовании не зафиксировано ни одного большого жизнеугрожающего кровотечения, а только события, не требующие значительного вмешательства в антикоагулянтную терапию. Возможно, среди пациентов, перенесших большие кровотечения, вероятные лабораторные предикторы геморрагических событий будут значительно больше отличаться от нормы.
Исследование, в значительной степени напоминающее дизайном наше, проведено в клинике Милана [16]. Регистр REGINA, включавший пациентов пожилого и старческого возраста с ФП и принимавших ПОАК, позволил провести проспективное наблюдение в течение 12 месяцев. Авторы не приводят сравнения пациентов, перенесших и не перенесших кровотечения, по показателям лабораторных тестов, однако отмечают, что значения шкал риска HAS-BLED и CHA2DS2-VASc достоверно не различались, что можно трактовать как потенциальную сопоставимость групп по данным лабораторных исследований.
Заключение
Результаты лабораторных исследований, в частности показателей уровня гемоглобина, тромбоцитов, а также креатинина и СКФ, имеют невысокую прогностическую значимость в отношении развития кровотечений у пациентов старческого возраста с ФП, принимающих ПОАК (дабигатран, ривароксабан и апиксабан).
Список литературы / References
- Филатов А.Г., Тарашвили Э.Г. Эпидемиология и социальная значимость фибрилляции предсердий. ФГБУ научный центр сердечно-сосудистой хирургии им. А.Н. Бакулева НАМН. Анналы аритмологии. 2012;9(2):5-13. Режим доступа: http://arrhythmology.pro/files/pdf/aa_02_2012_005-013_0.pdf / Filatov A.G., Tarashvili E.G. Overview. Epidemiology and social significance of atrial fibrillation. FSBI A.N. Bakulev Scientific Center for Cardiovascular Surgery NAMS. Annaly aritmologii = Annals of Arrhythmology. 2012;9(2):5-13. Available at: http://arrhythmology.pro/files/pdf/aa_02_2012_005-013_0.pdf
- Go A.S., Hylek E.M., Phillips K.A., Chang Y., Henault L.E., Selby J.V. et al. Prevalence of diagnosed atrial fibrillation in adults: national implications for rhythm management and stroke prevention: the AnTicoagulation and Risk Factors in Atrial Fibrillation (ATRIA) Study. JAMA. 2001;285(18):2370. doi: 10.1001/jama.285.18.2370.
- Heeringa J., van der Kuip D.A., Hofman A., Kors J.A., van Herpen G., Stricker B.H. et al. / Prevalence, incidence and lifetime risk of atrial fibrillation:the Rotterdam study. Eur Heart J. 2006;27(8):949- 53. doi: 10.1093/eurheartj/ehi825.
- Kumar K. Overview of atrial. Avaliable at: https://www.uptodate.com/contents/overview-of-atrial-fibrillation/print#!
- Stroke Risk in Atrial Fibrillation Working Group. Independent predictors of stroke in patients with atrial fibrillation: a systematic review. Neurology. 2007;69(6):546. doi: 10.1212/01.wnl.0000267275.68538.8d.
- Poli D., Antonucci E., Grifoni E., Abbate R., Gensini G.F., Prisco D. Bleeding risk during oral anticoagulation in atrial fibrillation patients older than 80 years. J Am Coll Cardiol. 2009;54(11):999-1002. doi: 10.1016/j.jacc.2009.05.046.
- Chao T.F., Liu C.J., Lin Y.J., Chang S.L., Lo L.W., Hu Y.F. et al. Oral Anticoagulation in Very Elderly Patients With Atrial Fibrillation: A Nationwide Cohort Study. Circulation. 2018;138(1):37. doi: 10.1161/ CIRCULATIONAHA.117.031658.
- Zoppellaro G., Zanella L., Denas G., Gennaro N., Ferroni E., Fedeli U. et al. Different safety profiles of oral anticoagulants in very elderly non-valvular atrial fibrillation patients: a retrospective propensity score matched cohort study. IJCA. 2018;265:103-107. doi: 10.1016/j.ijcard.2018.04.117.
- Fava J.P., Starr K.M., Ratz D., Clemente J.L. Dosing challenges with direct oral anticoagulants in the elderly: a retrospective analysis. Ther Adv Drug Saf. 2018; 9(8)405-414. doi: 10.1177/2042098618774498.
- Fumagalli S., Salah S.A.M., Laroche C., Gabbai D., Marchionni N., Boriani G. et al. Age-Related Differences in Presentation, Treatment, and Outcome of Patients With Atrial Fibrillation in Europe The EORP-AF General Pilot Registry (EURObservational Research Programme-Atrial Fibrillation). JACC: Clinical electrophysiology. 2015;1(4):326-334. doi: 10.1016/j.jacep.2015.02.019.
- Zhu W., He W., Guo L., Wang X., Hong K. The HAS-BLED Score for Predicting Major Bleeding Risk in Anticoagulated Patients With Atrial Fibrillation: A Systematic Review and Meta-analysis. Clin Cardiol. 2015;38(9):555-61. doi: 10.1002/clc.22435.
- Garcia D.A., Crowther M. Management of bleeding in patients receiving direct oral anti- coagulants. Available at: https://www.upto- date.com/contents/management-of-bleeding- in-patients-receiving-direct-oral-anticoagulants
- O'Brien E.C., Simon D.N., Thomas L.E., Hylek E.M., Gersh B.J., Ansell J.E., et al. The ORBIT bleeding score: a simple bedside score to assess bleeding risk in atrial fibrillation. European Heart Journal. 2015;36(46):3258–3264. doi: 10.1093/eurheartj/ehv476.
- Zhu W., He W., Guo L., Wang X., Hong K. The HAS-BLED Score for Predicting MajorBleeding Risk in Anticoagulated Patients With Atrial Fibrillation: A Systematic Review and Meta-analysis. Clin Cardiol. 2015;38(9):555-61. doi: 10.1002/clc.22435.
- Lutz J., Jurk K., Schinzel H. Direct oral anticoagulants in patients with chronic kidney disease: patient selection and special considerations. Int J Nephrol Renovasc Dis. 2017;10:135–143. doi: 10.2147/IJNRD.S105771.
- Monelli M., Molteni M., Cassetti G., Bagnara L., De Grazia V., Zingale L. et al. Non-vitamin K oral anticoagulant use in the elderly: a prospective real-world study – data from the REGIstry of patients on Non-vitamin K oral Anticoagulants (REGINA). Vasc Health Risk Manag. 2019;15:19–25. doi: 10.2147/VHRM.S191208.
Информация об авторах:
Габитова Мария Александровна, ассистент кафедры факультетской терапии № 1 Института клинический медицины, Федеральное государственное автономное образовательное учреждение высшего образования «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2
Крупенин Павел Михайлович, аспирант кафедры неврологии и нейрохирургии Института клинической медицины, Федеральное государственное автономное образовательное учреждение высшего образования «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2
Соколова Анастасия Андреевна, к.м.н., доцент кафедры факультетской терапии № 1 Института клинический медицины, Федеральное государственное автономное образовательное учреждение высшего образования «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2
Напалков Дмитрий Александрович, д.м.н., профессор кафедры факультетской терапии № 1 Института клинический медицины, Федеральное государственное автономное образовательное учреждение высшего образования «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет);119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2
Фомин Виктор Викторович, д.м.н., член-корреспондент РАН, заведующий кафедрой факультетской терапии № 1 Института клинический медицины, Федеральное государственное автономное образовательное учреждение высшего образования «Первый Московский государственный медицинский университет имени И.М. Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский Университет); 119991, Россия, Москва, ул. Трубецкая, д. 8, стр. 2
Information about the author:
Mariia A. Gabitova, Assistant of the Department of Faculty Therapy No. 1 of the Institute of Clinical Medicine, Federal State Autonomous Educational Institution of Higher Education «I.M. Sechenov First Moscow State Medical University» of the Ministry of Health of the Russian Federation (Sechenov University); 8-2, Trubetskaya st., Moscow, 119991, Russia
Pavel M. Krupenin, postgraduate student of the Department of Neurology and Neurosurgery of the Institute of Clinical Medicine, Federal State Autonomous Educational Institution of Higher Education «I.M. Sechenov First Moscow State Medical University» of the Ministry of Health of the Russian Federation (Sechenov University); 8-2, Trubetskaya st., Moscow, 119991, Russia
Anastasiya A. Sokolova, Cand. of Sci. (Med), Associate Professor of the Department of Faculty Therapy No. 1 of the Institute of Clinical Medicine, Federal State Autonomous Educational Institution of Higher Education «I.M. Sechenov First Moscow State Medical University» of the Ministry of Health of the Russian Federation (Sechenov University); 8-2, Trubetskaya st., Moscow, 119991, Russia
Dmitriy A. Napalkov, Dr. of Sci. (Med), Professor of the Department of Faculty Therapy No. 1 of the Institute of Clinical Medicine, Federal State Autonomous Educational Institution of Higher Education «I.M. Sechenov First Moscow State Medical University» of the Ministry of Health of the Russian Federation (Sechenov University); 8-2, Trubetskaya st., Moscow, 119991, Russia
Viktor V. Fomin, Dr. of Sci. (Med), Corresponding Member of the RAS, Head of the Department of Faculty Therapy No. 1 of the Institute of Clinical Medicine, Federal State Autonomous Educational Institution of Higher Education «I.M. Sechenov First Moscow State Medical University» of the Ministry of Health of the Russian Federation (Sechenov University); 8-2, Trubetskaya st., Moscow, 119991, Russia




 1
1 2
2 3
3 4
4


Комментарии (0)